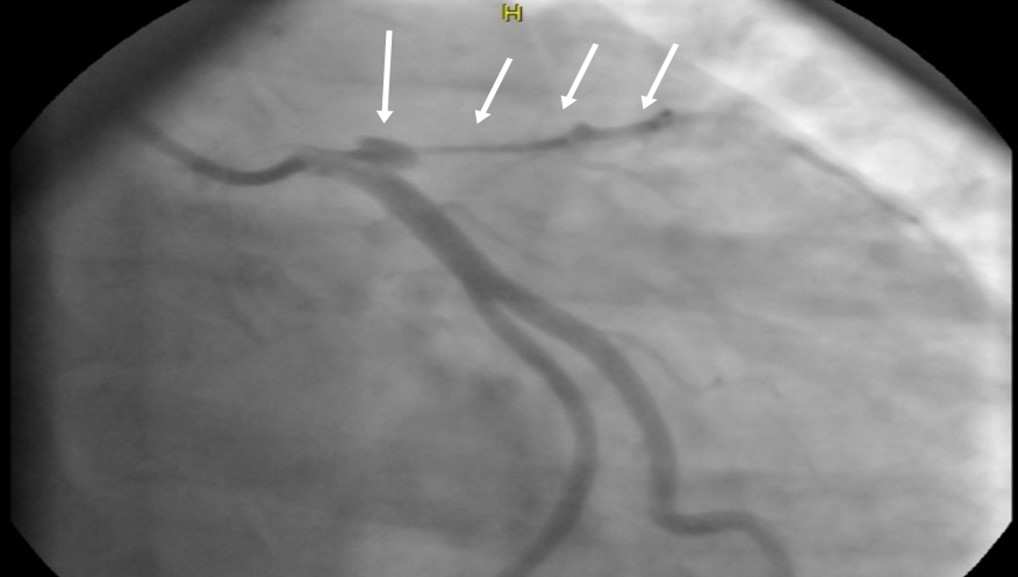
ЕКГ знахідки після трансплантації серця
ЕКГ після трансплантації серця. КлінКейсКвест Академія [Internet]: ClinCaseQuest Publishing; 2021(12). 7 грудня 2021.
Трансплантація серця
Першу трансплантацію серця людини здійснив Крістіан Барнард у 1967 році. З того часу проведення трансплантації серця є додатковою важливою лікувальною стратегією для безнадійних пацієнтів.
Існують дві хірургічні процедури для трансплантації серця: ортотопічна трансплантація серця і гетеротопічна трансплантація серця. Ортотопічна є більш поширеною та стандартною технікою, при якій нативне серце замінюється донорським [1-9]. Через збереження задньої стінки правого передсердя реципієнта, включаючи нативний синоатріальний вузол, на ЕКГ можуть бути виявлені два набори зубців P з різною частотою (подвійні синусові вузли), але до шлуночків можуть проводитися тільки зубці P серця донора. Однак у деяких випадках через малу амплітуду зубця P залишків передсердя реципієнта може спостерігатися лише один зубець P. При гетеротопічній трансплантації серця, яка рідше використовується, нативне серце залишається на місці, а донорське серце розташоване поруч із серцем реципієнта, зазвичай в правій частині грудної клітини, а поверхнева ЕКГ показує накладені ритми рідного і донорського серця, яке представлено праворуч. Розділення двох сердець у їхньому ритмі може викликати подвійний ритм у подвійному серці. Повідомлялося про фібриляцію шлуночків нативного серця та синусовий ритм донорського серця у пацієнта з гетеротопною трансплантацією.
Гетеротопна трансплантація була корисною до покращення режимів імуносупресії та механічної підтримки кровообігу, оскільки допомагала підтримувати кровообіг у випадках гострої недостатності трансплантата. Зараз ця технологія рідко використовується і обмежується окремими пацієнтами, включаючи випадки з незворотньою легеневою гіпертензією та пацієнтів із вираженою невідповідністю розміру донор-реципієнт. До недоліків цієї методики можна віднести тривалість і складність операції, ателектаз внаслідок здавлення нижньої частки правої легені серцем донора, збільшення частоти тромбоемболій, рецидивів стенокардії, аритмії, утруднення біопсії ендоміокарда, ендокардиту. Отже ортотопічна трансплантація стає найбільш поширеною технікою.
Ортотопічна трансплантація серця є найефективнішою довготривалою терапією термінальної стадії серцевої недостатності з імплантованими допоміжними пристроями лівого шлуночка як альтернатива для окремих пацієнтів. За даними Міжнародного товариства трансплантації серця і легенів (ISHLT), з кожним роком кількість пацієнтів з ортотопічною трансплантацією серця збільшується. У міру вдосконалення хірургічних методів та імуносупресивних режимів короткочасна смертність, спричинена сепсисом, зменшилась, тоді як захворюваність, спричинена повторними епізодами відторгнення та васкулопатією серцевого алотрансплантата, зросла і часто проявляється аритміями.
Серця, відібрані для проведення ортотопічної трансплантації, повинні бути в хорошому стані і в цілому битися в синусовому ритмі. Тривалий час ішемії трансплантата може спричинити пошкодження провідної системи в ранні та пізні періоди після трансплантації серця. Періопераційне ішемічне ураження та подальший ендокардіальний фіброз, ймовірно, відіграють механістичну роль у багатьох випадках. Пацієнти з тривалою ішемією трансплантата (>4 години) класифікуються як групи високого ризику та мають більший рівень 30-денної та річної смертності. Ризик хронічного відторгнення внаслідок посиленої активації ендотелію судин трансплантата також може збільшуватися, якщо збереження міокарда не є адекватним.
З огляду на початок програми трансплантації в Україні та досягнуті успіхи вітчизняних команд трансплантації донорських органів ми наводимо огляд даних клінічних досліджень, які стосувалися змін ЕКГ після трансплантації серця, що може бути корисним фахівцям, які залучені у подальше спостереження за такими пацієнтами: сімейні лікарі, кардіологи первинної та вторинної медичної допомоги.
Ретельний моніторинг електрокардіограми (ЕКГ) вважається одним з важливих методів спостереження у осіб, яким було проведено трансплантацію серця.
Зниження вольтажності QRS, розвиток атріовентрикулярної блокади або затримки внутрішньошлуночкової провідності відзначалися у експериментальних тварин як ранні ознаки імунологічного відторгнення донорського серця. Останнім часом роль ЕКГ при гострому відторгненні є спірною. Але своєчасна оцінка та вірна інтерпретація даних ЕКГ залишається важливою поруч з іншими методами кардіологічного моніторингу при наданні допомоги хворим після трансплантації серця.
Електрокардіографічні зміни описані після трансплантації серця майже у 75% пацієнтів. У ранньому післяопераційному періоді зазвичай виявляють порушення провідності, які в 3-5% потребують імплантації кардіостимулятора. Найбільш частим персистуючим розладом є блокада правої ніжки пучка Гіса, яка має клінічне значення лише тоді, коли має прогресуючий характер. Частота післяопераційної фібриляції або тріпотіння передсердь нижча в порівнянні з іншими кардіохірургічними операціями, і їх раптовий розвиток може бути пов’язаний з гострим відторгненням. Шлуночкові аритмії розвиваються, як правило, як ускладнення запущеної ішемічної хвороби трансплантата і часто є причиною раптової смерті. До введення циклоспорину А відносно надійною ознакою гострого відторгнення було зниження вольтажності комплексу QRS. При сучасному лікуванні зміни ЕКГ розвиваються лише при важких формах відторгнення, початкові зміни можна зафіксувати лише за допомогою внутрішньосерцевої електрограми.
Анатомічні особливості функціонування трансплантованого серця
Власне серце інервується симпатичними та парасимпатичними волокнами нервової системи. Трансплантація призводить до перетину цих волокон, денервуючи алотрансплантат та змінюючи його фізіологію. Пересаджене серце денервовано і не має автономного нейронного контролю. Денервоване серце викликає зміни на електрокардіограмі (ЕКГ) реципієнтів пересадженого серця [1]. У пацієнтів після трансплантації серця є схильність до підвищення частоти серцевих скорочень у стані спокою. Позбавлений центрального впливу синусовий вузол пересадженого серця забезпечує збільшену порівняно з нормою ЧСС – у спокої до 90-110 ударів/хв. Крім того, реєструється зниження здібності до варіації частоти серцевих скорочень протягом 24 годин. Денервація змінює відповідь серця на зовнішні впливи, що діють безпосередньо через автономну нервову систему серця. Безпосередньо після трансплантації серця спостерігається повна вегетативна дисфункція, що відповідає тяжкості перенесеної операції та повної симпатоадреналової блокади донорського органу. Поява окремих спектральних компонентів варіабельності серцевого ритму (ВСР) у реабілітаційному періоді можна інтерпретувати як відображення процесу реіннервації. З часом відбувається як симпатична, так і парасимпатична реіннервація, але ступінь реіннервації є неповним, неоднорідним, відрізняється між пацієнтами та неоднорідний у одного пацієнта. Насамперед відновлюються гуморальні відділи регуляції серцевого ритму. Відсутність позитивної динаміки параметрів ВСР, очевидно, можна розцінювати, як одну з ознак реакції відторгнення донорського органу.
Неостигмін, панкуроній, опіоїди не впливають на частоту серцевих скорочень, а дигоксин неефективний при тахікардії. При аналізі ЕКГ іноді виявляється другий зубець P, що походить з активованого передсердного залишку реципієнта. Проте найбільш частою знахідкою ЕКГ після трансплантації серця є блокада правої ніжки пучка Гіса.
При проведенні трансплантації реципієнт зберігає задні стінки власних передсердь. Передсердя реципієнта васкуляризовані бронхіальними колатеральними судинами.
Зміни ЕКГ у цих пацієнтів в основному зумовлені залишковою активністю передсердь реципієнта, пошкодженням серця донора під час процедури трансплантації та опіром легеневих судин перед трансплантацією у реципієнта (PVR).
ЕКГ знахідки після трансплантації серця
Після трансплантації серця можуть виникнути різноманітні аритмії. Основні механізми аритмій у трансплантованому серці пов’язані з хірургічним втручанням, відторгненням або васкулопатією серцевого алотрансплантата, попереднім впливом препаратів реципієнта або самим трансплантованим серцем. Після трансплантації може розвиватися ішемічна хвороба серця та васкулопатія серцевого алотрансплантата, які також, в свою чергу, можуть викликати аритмії.
Затримка внутрішньошлуночкової провідності або блокада правої ніжки пучка Гіса переважає у реципієнтів із трансплантатом серця протягом першого року після операції з трансплантації. Критерії ЕКГ щодо збільшення передсердя (особливо лівого передсердя) також є поширеним явищем і, ймовірно, пов’язані з операцією з трансплантації з подальшим ремоделюванням передсердь.
David Pickham і співавтори опублікували результати спостереження за пацієнтами після трансплантації серця, метою яких було дослідження особливостей змін ЕКГ після трансплантації [1]. Результати дослідження продемонстрували, що синусовий ритм або синусова тахікардія переважають у перший рік після трансплантації серця. У вибірці спостереження з 98 пацієнтів надшлуночкові аритмії були рідкісними (<1%), а шлуночкові аритмії або AV-блокада другого/третього ступеня не реєструвалися.
Було виявлено, що найпоширенішою аномалією ЕКГ була затримка або блокада внутрішньошлуночкової провідності, що зустрічалася у 69% пацієнтів. Етіологія та клінічне значення затримки внутрішньошлуночкової провідності або блокади правої ніжки пучка Гіса неясні; це може бути ознакою розтягнення правого шлуночка та його ремоделювання у пацієнтів із тяжкою серцевою недостатністю, що потребує трансплантації. Проте досліджувана когорта пацієнтів не мала необоротної легеневої гіпертензії перед операцією, оскільки всі вони мали ізольовану трансплантацію серця (тобто були виключені пацієнти з трансплантацією серця та легенів).
Деякі дослідження пов’язують затримку внутрішньошлуночкової провідності справа або блокаду правої ніжки пучка Гіса зі збільшенням смертності в популяції після трансплантації [10,11], тоді як інші не виявили такої кореляції [12–14]. У суб-аналізі осіб з трансплантацією серця із затримкою внутрішньошлуночкової провідності праворуч Гао та його колеги [15] продемонстрували більш високий рівень внутрішньосерцевого тиску у тих, хто має затримки внутрішньошлуночкової провідності, ніж без неї. Однак тиск залишався в прийнятних межах і, таким чином, не зміг адекватно пояснити це явище. Маркус та ін. провели одне з найбільш масштабних досліджень на сьогодні з 322 реципієнтами пересадки серця, за якими спостерігали протягом 9 ±3 років [14]. Вони виявили, що затримка внутрішньошлуночкової провідності праворуч або блокада правої ніжки пучка Гіса розвивалися з часом, і тому заперечували периопераційну причину. Однак Джессен та його колеги виявили, що затримки внутрішньошлуночкової провідності або блокади правої ніжки пучка Гіса присутні відразу після операції, надавши аргумент, що геометричні та обертальні сили сприяли цим порушенням провідності [13]. Іншими постулюваними механізмами для раннього розвитку затримки внутрішньошлуночкової провідності праворуч є інтраопераційні фактори, такі як збільшення часу ішемії трансплантата [16,17].
Можна припустити, що затримки/блокади внутрішньошлуночкової провідності були присутні у донора до трансплантації. Однак аргументом проти високої поширеності затримки внутрішньошлуночкової провідності або блокади правої ніжки пучка Гіса, що виникли від донора, є нещодавній аналіз 980 ЕКГ з Каліфорнійської мережі донорів трансплантації, який повідомив, що 97% донорів мали нормальну внутрішньошлуночкову провідність на ЕКГ перед трансплантацією [18].
Другою за поширеністю аномалією ЕКГ, яка спостерігалася в наведеному дослідженні Pickham D. та співавторів, було збільшення передсердь, яке виявлялося у 64% випадках [1]. Можливе пояснення цієї знахідки може бути пов’язане з хірургічною технікою стандартної ортотопічної трансплантації серця [19], яка включає трансплантацію шлуночків донора та частини переднього передсердя до нативної задньої та бічної стінок передсердь реципієнта. Було показано, що це призводить до збільшення порожнин передсердь аномальної форми та утворення помітної лінії шва між компонентами реципієнта та донора [20]. Тому поясненням високої поширеності позитивних критеріїв ЕКГ для збільшення передсердь після трансплантації може бути комбінація нативних уражень задньої стінки передсердь та хірургічні рубці, а не прогресування захворювання у пацієнта після хірургічної трансплантації [21].
В альтернативному поясненні Cui G та його колег [22], які вивчали зв’язок між відторгненням клітинного алотрансплантата після трансплантації серця та змінами критеріїв зубця Р для збільшення лівого передсердя у відведенні V1, повідомляється про те, що аномальна деполяризація лівого передсердя була багатогранною; зміни зубця P не корелювали ні з розміром лівого передсердя, ні з тиском, ні з системною гіпертензією, і, таким чином, не вказували на збільшення передсердя. Ці дослідники виявили, що лише ступінь клітинного відторгнення корелювала із критеріями зміни зубця P. Запропонованим механізмом цієї кореляції є пошкодження клітин міокарда та порушення у структурі волокон міокарда під час клітинного відторгнення, що призводить до неоднорідної провідності та аномалій зубця P.
Третя аномалія ЕКГ, яка була присутня у 23% пацієнтів, була пов’язана з зубцем Q, що відповідала критеріям інфаркту міокарда.
Але
а) не всі зубці Q є патологічними;
b) не всі патологічні зубці Q викликані інфарктом міокарда;
c) немає твердого консенсусу щодо діагностики патологічних зубців Q.
Також в літературі описані наступні зміни на ЕКГ після трансплантації серця та їх можливе пояснення:
| ЕКГ знахідка | Інтерпретація |
| Два зубці P | Нативні зубці P реципієнта мають невелику амплітуду. Донорські зубці P мають нормальну амплітуду і конфігурацію. Шовна лінія між передсердями донора та реципієнта блокує будь-який обмін електричними імпульсами від двох джерел. Присутня дисоціація передсердь. Донорський зубець Р проводиться і стимулює шлуночки. Передсердні імпульси реципієнтів не проводяться. Швидкість денервованого серця донора вища, ніж частота залишкових передсердь реципієнта. Зубці P залишків передсердь реципієнта можуть не спостерігатися через їх малу амплітуду або наявність дисфункції синусового вузла або фібриляцію передсердь до трансплантації, або втрату артерії синусового вузла під час операції. Фібриляція/тріпотіння може бути присутнім в одній групі передсердь, тоді як нормальний синусовий ритм присутній в іншій парі, що ускладнює інтерпретацію. |
| Повна або неповна блокада правої ніжки пучку Гіса | Зустрічається у 45-83% пацієнтів після трансплантації. |
| Ліва передня фасцикулярна блокада | Фасцикулярні блокади представлені блокадою передньої гілки лівої ніжки пучка Гіса. Розвивається у 25% пацієнтів. |
| Брадіаритмії через дисфункцію синусового вузла | Брадіаритмії виникають у 8-23% пацієнтів після ортотопічної трансплантації серця. Причина розвитку не пояснюється відторгненням або ішемічним періодом під час трансплантації. Тимчасові кардіостимулятори можуть бути ненадійними у забезпеченні ритму, і може настати раптова смерть, може знадобитися імплантація постійного кардіостимулятору. У більшості випадків основним ускладненням є дисфункція синусового вузла; однак також може виникнути AV-блокада. Передопераційне застосування аміодарону у пацієнта-реципієнта також може призвести до посттрансплантаційної брадикардії. У пацієнтів із пізнім початком симптоматичної брадикардії слід виключити відторгнення та ІХС трансплантата або васкулопатію серцевого алотрансплантата. Атропін неефективний при брадиаритміях, оскільки серце денервовано. |
| Шлуночкові екстрасистолії | Можуть бути пов’язані з атеросклерозом коронарних судин трансплантату. |
| Передчасні передсердні комплекси, пароксизмальна суправентрикулярна тахікардія, фібриляція та тріпотіння передсердь | Деякі дослідники раніше вважали, що ці епізоди пов’язані з епізодами відторгнення. Передсердна тахікардія виникає переважно у верхньому правому передсерді, навколо лінії нативного та донорського шва, що потребує проведення аблації. Хірургічні рубці на лініях передсердних швів можуть утворювати ділянки сповільненої провідності. Предсердна провідникова тахікардія від реципієнта до донора також зазвичай включала анастомоз правого передсердя. У цих випадках абляцію було успішно проведено на місці найранішої активації передсердь донора на лінії шва. Крім того, тахікардія реципієнта або передсердний ритм із блокуванням виходу до донорського передсердя можуть викликати у лікарів складнощі інтерпретації ЕКГ, яка демонструє подвійну передсердну тахікардію, псевдоатріовентрикулярну блокаду або псевдопередсердну тахікардію з двома різними передсердними морфологічними хвилями від донора та від реципієнта. Найпоширеніша аритмія після трансплантації серця – тріпотіння передсердь (9%) і стійка або пароксизмальна фібриляція передсердь (ФП; 7%); 57% ФП виникли в періопераційному періоді. ФП вкрай рідко зустрічається у стабільних пацієнтів у довгостроковій перспективі після трансплантації; коли це відбувається, пізня ФП може бути спричинена гострим або хронічним відторгненням, васкулопатією або сепсисом. Насправді, ФП є рідкісною знахідкою після трансплантації серця в порівнянні з іншими хірургічними втручаннями і скоріше пов’язана з гострим відторгненням. |
| АВ тахікардія та АВ вузлова re-entry тахікардія | Іноді АВ тахікардія та АВ вузлова re-entry тахікардія може виникати у пацієнтів з пересадженим серцем, навіть якщо донор ніколи не відчував тахікардії чи аритмії; зміни вегетативного тонусу, що впливають на субстрат, ймовірно, є механізмом тахікардії у пацієнта-реципієнта. |
| Зміни сегмента ST і зубця Т | У деяких пацієнтів в ранньому післяопераційному періоді може розвинутися дифузний підйом сегмента ST з подальшими еволюційними змінами сегмента ST і зубця Т, що відповідає гострому перикардиту. Як правило, ці зміни є тимчасовими. У деяких пацієнтів розвиваються ішемічні зміни зубця Т, які не пов’язані з ознаками гострого відторгнення, і ангіографія не виявляє змін. Прискорений атерогенез. У 40% пацієнтів ознаки атеросклерозу спостерігаюється через три роки, так само часто у тих, хто мав і не мав ішемічної хвороби серця на момент трансплантації. Вважається, що механізмом пошкодження є імунологічне пошкодження коронарного ендотелію. Атерослеротична хвороба серця проявляється проксимальними ураженнями і дифузним облітеруючим захворюванням. Зазвичай має безсимптомний перебіг через денервацію. |
| ЕКГ докази відторгнення | Хоча спочатку низька вольтажність вказувала на відторгнення, але це було поставлено під сумнів. |
| Безпульсова електрична активність (PEA) | З ретроспективних досліджень відомо, що форма прояву РСС у переважної більшості пацієнтів із трансплантованим серцем це безпульсова електрична активність (PEA) на відміну від фібриляції шлуночків. |
| Синдром Такоцубо | Описані поодинокі випадки розвитку синдрому Такоцубо у реципієнта. |
Виникнення аритмії під час спостереження після трансплантації асоціюються з гіршими результатами через гостре відторгнення, дисфункцію лівого шлуночка (ЛШ) та раптову серцеву смерть (РСС).
З огляду на те, що подовження інтервалу QTc вважається фактором ризику несприятливого прогнозу в загальній популяції без трансплантації, її прогностична цінність у реципієнтів трансплантата серця була недостатньо вивчена.
В одному з досліджень [4] вивчалось чи подовжений інтервал QTc є предиктором несприятливого прогнозу у реципієнтів трансплантата серця. Було встановлено, що відносне збільшення тривалості інтервалу QTc на ≥10% між першим і другим роком після трансплантації є сильним, незалежним предиктором смертності у реципієнтів пересадженого серця. Тож моніторинг QTc є важливим для пацієнтів із трансплантатом серця.
Висновки
Багато центрів серця проводять трансплантацію серця по всьому світу. Реципієнту показані регулярні контрольні огляди та обстеження, включаючи ехокардіограму, електрокардіограму. Розуміння ЕКГ знахідок, їх інтерпретація у реципієнтів пересадженого серця має клінічне значення для забезпечення спостереження за хворими.
Зареєструйтеся на нашому сайті прямо зараз, щоб мати доступ до більшої кількості навчальних матеріалів!
Підписатися на наші сторінки:
Також читати:
Джерела:
- Pickham D, Hickey K, Doering L, Chen B, Castillo C, Drew BJ. Electrocardiographic abnormalities in the first year after heart transplantation. J Electrocardiol. 2014;47(2):135-139. doi:10.1016/j.jelectrocard.2013.09.006
- Villa AE, de Marchena EJ, Myerburg RJ, Castellanos A. Comparisons of paired orthotopic cardiac transplant donor and recipient electrocardiograms. Am Heart J. 1994 Jan; 127(1):70-4.
- Jessup M, Drazner MH, Book W, Cleveland JC Jr. 2017 ACC/AHA/HFSA/ISHLT/ACP Advanced Training Statement on Advanced Heart Failure and Transplant Cardiology (Revision of the ACCF/AHA/ACP/HFSA/ISHLT 2010 Clinical Competence Statement on Management of Patients With Advanced Heart Failure and Cardiac Transplant): A Report of the ACC Competency Management Committee. Circ Heart Fail. 2017 Jun;10(6):e000021. doi: 10.1161/HHF.0000000000000021. Erratum in: Circ Heart Fail. 2018 May;11(5):e000028. PMID: 28607153.
- Bojan Vrtovec, Rajko Radovancevic, Cynthia D. Thomas et al. Prognostic Value of the QTc Interval after Cardiac Transplantation. Clinical heart transplantation. Vol. 25 (1), P29-35, JANUARY 01, 2006 Published:November 21, 2005 DOI:https://doi.org/10.1016/j.healun.2005.05.004
- Hosková L, Málek I, Krausová R, Podzimková M, Pirk J. Elektrokardiografické zmĕny po transplantaci srdce [Electrocardiographic changes after heart transplantation]. Vnitr Lek. 2002 Dec;48 Suppl 1:72-5. Czech. PMID: 12744023.
- Hamon D, Taleski J, Vaseghi M, Shivkumar K, Boyle NG. Arrhythmias in the heart transplant patient. Arrhythm Elctrophysiol Rev. 2014;3:149-55.
- Khush KK, Cherikh WS, Chambers DC, Goldfarb S, Hayes D Jr, Kucheryavaya AY, Levvey BJ, Meiser B, Rossano JW, Stehlik J; International Society for Heart and Lung Transplantation. The International Thoracic Organ Transplantation Registry of the International Society for Heart and Lung Transplantion: Thirty-Fifth Adult Heart Transplantation Report-2018; Focus Theme: Multiorgan Transplantation. J Heart Lung Transplant. 2018;37:1155-1168.
- Baretti R, Debus B, Lin BS, Weng YG, Pasic M, Hübler M, Grauhan O, Knosalla C, Dandel M, Kemper D, Hiemann N, Lehmkuhl HB, Hetzer R. Arrhythmia post heart transplantation. Applied Cardiopulmonary Pathophysiology. 2011;15:256-71.
- Russo MJ, Chen JM, Sorabella RA, Martens TP, Garrido M, Davies RR, George I, Cheema FH, Mosca RS, Mital S, Ascheim DD, Argenziano M, Stewart AS, Oz MC, Naka Y. The effect of ischemic time on survival after heart transplantation varies by donor age: an analysis of the United Network for Organ Sharing database. J Thorac Cardiovasc Surg. 2007;133:554-9.
- Osa A, Almenar L, Arnau MA, et al. Is the prognosis poorer in heart transplanted patients who develop a right bundle branch block? The Journal of Heart and Lung Transplantation. 2000;19(2):207–214. (читати)
- Leonelli FM, Dunn JK, Young JB, Pacifico A. Natural history, determinants, and clinical relevance of conduction abnormalities following orthotopic heart transplantation. The American Journal of Cardiology. 1996;77(1):47–51. (читати)
- Golshayan D, Seydoux C, Sillard Berguer D, et al. Incidence and prognostic value of electrocardiographic abnormalities after heart transplantation. Clinical Cardiology. 1998;21:680–684. (читати)
- Jessen ME, Olivari M-T, Wait MA, Meyer DM, Yancey CW, Jr, Ring WS. Frequency and significance of right bundle branch block after cardiac transplantation. The American Journal of Cardiology. 1994;73(13):1009–1011. (читати)
- Marcus GM, Hoang KL, Hunt SA, Chun SH, Lee BK. Prevalence, Patterns of Development, and Prognosis of Right Bundle Branch Block in Heart Transplant Recipients. The American Journal of Cardiology. 2006;98(9):1288–1290. (читати)
- Gao S-z, Hunt SA, Wiederhold V, Schroeder JS. Characteristics of serial electrocardiograms in heart transplant recipients. American Heart Journal. 1991;122(3, Part 1):771–774. (читати)
- Leonelli FM, Pacifico A, Young JB. Frequency and significance of conduction defects early after orthotopic heart transplantation. The American Journal of Cardiology. 1994;73(2):175–179. (читати)
- Yamamoto S, Bergsland J, Michalek SM. Evolution of right bundle branch block and other intraventricular conduction abnormalities in the transplanted human heart. Japanese circulation journal. 1990;54(9):1122–1129. 1990/09/20. (читати)
- Khush K, Menza R, Nguyen J, Goldstein B, Zaroff J, Drew B. Electrocardiographic characteristics of potential organ donors and associations with cardiac allograft use. Circulation Heart Failure. 2012;5:475–483. (читати)
- Shumway N, Lower RS, RC Transplantation of the heart. Advanced Surgery. 1966;2:265–284. (читати)
- Angermann C, Spes C, Tammen A, et al. Anatomic characteristics and valvular function of the transplanted heart: transthoracic versus transesophargeal echocardiographic findings. Journal of Heart Transplantation. 1990;9(4):331–338. (читати)
- Young JB, Leon CA, Short HD, et al. Evolution of hemodynamics after orthotopic heart and heartlung transplantation: early restrictive patterns persisting in occult fashion. The Journal of heart transplantation. 1987;6(1):34–43. (читати)
- Cui G, Kobashigawa J, Chung T, Sen L. Atrial conduction disturbance as an indicator of rejection after cardiac transplantation. Transplantation. 2000;70(1):223–227. (читати)
Консультація пацієнта із спонтанною дисекцією коронарних судин – рекомендації ОСКІ
Автори: Hanna Samoilova, Nataliia Lopina Початок консультації Вимийте руки та при необхідності надіньте ЗІЗ (засоби…
Cимптомна брадикардія
Симптомна брадикардія виникає при зниженні частоти серцевих скорочень менше 50 ударів за хвилину. Найчастіше в…
Шлуночкові тахікардії
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров Клінічна термінологія Шлуночкову тахікардію визначають як три або…
Тромбоемболія легеневої артерії
Тромбоемболія легеневої артерії (ТЕЛА) ‒ це загрозливе для життя захворювання, обумовлене оклюзією стовбура чи гілок…
Проведення експрес тесту на визначення маркерів некрозу міокарду
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров У пацієнтів з ГКС може буде позитивний експрес-тест…
Гострий коронарний синдром без елевації сегменту ST
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров Визначення Гострий коронарний синдром – це група симптомів…