Фібриляція передсердь

Автори: Т.С. Заїкіна, Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров
Фібриляція передсердь (ФП) – це суправентрикулярна тахіаритмія, яка характеризується нерегулярною передсердною електричною активацією, що призводить до неефективного скорочення передсердь.
Фібриляція передсердь – це найчастіша надшлуночкова тахіаритмія, ознаками якої є швидка (350–700/хв), некоординована активація передсердь, що призводить до втрати гемодинамічної ефективності їх скорочень, що супроводжується нерегулярним ритмом шлуночків.
Фібриляція передсердь є найбільш поширеною формою стійкої аритмії серед дорослих у всьому світі, яка робить суттєвий внесок у збільшення рівня захворюваності та смертності.
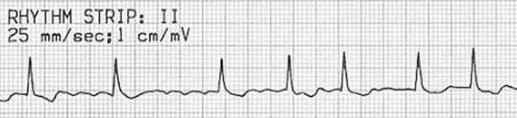
Електрокардіографічними ознаками ФП є:
- нерегулярні інтервали RR;
- відсутність синусових зубців Р;
- нерегулярна передсердна активність (f-хвиля).
Рисунок 1. Фібриляція передсердь. Зображення інтернет-ресурсу liftl.com
Для достовірного підтвердження цих ЕКГ-ознак ФП необхідно зареєструвати стандартну ЕКГ в 12 відведеннях або ритмограму тривалістю принаймні 30 секунд.
Епідеміологія
У всьому світі ФП є найпоширенішою тривалою серцевою аритмією у дорослих. ФП пов’язана зі значною захворюваністю та смертністю, що створює значне навантаження для пацієнтів, суспільного здоров’я та економіки охорони здоров’я. Наразі оцінена поширеність ФП серед дорослих становить від 2% до 4%, і очікується 2,3-разове зростання через тривалий період довголіття в загальній популяції та активізація пошуку недіагностованої ФП. Зростання віку є помітним фактором ризику ФП, але збільшується навантаження інших супутніх захворювань, включаючи гіпертензію, цукровий діабет, серцеву недостатність (СН), ішемічну хворобу серця (ІХС), хронічну хворобу нирок (ХХН), ожиріння та обструктивне апное сну. Модифіковані фактори ризику є значними факторами розвитку та прогресування ФП. Захворюваність, поширеність з урахуванням віку, та довічний ризик ФП нижчий у жінок порівняно з чоловіками та в когортах не європеоїдної та європеоїдної раси. Попередня оцінка ризику ФП протягом життя в 1 з 4 осіб була нещодавно переглянута до 1 з 3 осіб європейського походження при індексному віці 55 років. Ризик виникнення ФП протягом життя залежить від віку, генетичних та (суб)клінічних факторів. Спостережуваний вплив навантаження клінічного фактора ризику/численних супутніх захворювань на ризик ФП свідчить про те, що раннє втручання та модифікований контроль факторів ризику можуть зменшити випадки ФП.
Етіологія
ФП – це мультифакторне захворювання, в розвитку якого важливу роль грає комплексна взаємодія різних чинників, зокрема:
- демографічні фактори (вік, чоловіча стать, етнічна приналежність до жителів Кавказу, низький соціоекономічний статус);
- поведінкові звички, що стосуються здоров’я (паління, зловживання алкоголем, гіподинамія або надмірна фізична активність, заняття професійним спортом, надмірне вживання кофеіну);
- серцево-судинні захворювання (серцева недостатність, клапанні вади серця, вроджені вади серця, ішемічна хвороба серця);
- субклінічний атеросклероз (індекс кальцифікації коронарних артерій, потовщення інтіми-медії каротидних артерій або бляшка каротидних артерій);
- порушення ритму серця та провідності (синдром слабкості синусового вузла, подовження інтервалу PQ, синдром ВПВ);
- інші захворювання та преморбідні стани (гіпертензія, порушення ліпідного профілю, цукровий діабет та предіабет, порушення функції нирок, ожиріння, підвищення ІМТ, синдром обструктивного апное сну, хронічне обструктивне захворювання легень);
- генетичні фактори (обтяжений сімейний анамнез щодо ФП, короткий інтервал QT);
- запальний процес (підвищення СРБ, фібриногену, аутоімунні стани);
- інші (забруднення повітря, сепсис, несприятливий психологічний стан).
Фібриляція передсердь найчастіше розвивається у людей похилого віку. За статистикою, її діагностують у 10% населення старше 80 років. Але в молодому віці хвороба також зустрічається, особливо при наявності факторів ризику. Фібриляція передсердь може розвинутися на тлі інших захворювань серця або внутрішніх органів, а також у повністю здорових людей.
Предиктори ФП:
Фібриляція передсердь може виникати при різних серцевих та позасерцевих захворюваннях. До серцевих причин ФП можна віднести:
- Артеріальна гіпертензія
- Набуті вади клапанів (особливо значущими є вади мітрального клапана)
- Вроджені вади серця (дефекти міжпередсердної перегородки)
- Серцева недостатність
- Ішемічна хвороба серця
- Дилатаційна кардіоміопатія
- Гіпертрофічна кардіоміопатія
- Запальні захворювання серця:
- Міокардит
- Перекардит
- Синдром слабкості синового вузла
- Синдром преекзитації
- Саркоїдоз серця
- Амілоїдоз серця
- Гемохроматоз серця
- Новоутворення серця
До позасерцевих причин ФП можна віднести:
- Гіпертиреоз (дуже часто)
- Гіпотиреоз
- Гострі інфекційні захворюваання (наприклад, Covid-19)
- Загальний наркоз
- Захворювання легень
- Ниркові (феохромоцитома, хронічне захворювання нирок)
- Ожиріння
- Цукровий діабет
- Метаболічний синдром,
- Професійне заняття спортом
- Дія токсични речовин (алкоголь, окис вуглецю, лікарські засоби)
Патофізіологія
На даний час вважається, що патогенез ФП зумовлений взаємодією між ініціюючим тригером, часто у формі ектопічного вогнища електричного збудження, розташованого в одній або декількох легеневих венах, і аномальним тканинним субстратом в передсерді, здатним підтримувати цю аритмію.
Наразі відомо, що ектопічні вогнища електричного збудження найчастіше розташовуються в м’язових рукавах, які поширюються від лівого передсердя до проксимальних відділів легеневих вен, та відіграють ключову роль у ініціації ФП. Механізми, задіяні у створенні ектопічної електричної активності цими рукавами, а також точний механізм ініціації ФП залишаються до кінця не з’ясованими. Існує думка, що механізми ініціації ектопічної вогнищевої активності включають підвищений автоматизм, тригерну активність та мікро-реентрі. Також під час штучної ініціації пароксизму ФП було виявлено зміни у вегетативному тонусі від різкого підвищення симпатичної активності до швидкого переходу до підвищеної парасимпатичної активності.
Для збереження ФП необхідний аномальний тканинний субстрат у міокарді передсердя, тобто структурна аномалія міокарда передсердь, яка дозволить циркулювати патологічним електричним імпульсам. Хоча у більшості випадків ФП виникає у пацієнтів зі структурною патологією серця (аномальним тканинним субстратом), ця аритмія може розвиватися і у пацієнтів молодого віку без структурної патології серця за рахунок високої активності тригера легеневої вени. Переважання того чи іншого патофізіологічного чинника впливає на перебіг ФП: пацієнти без структурної патології серця, як правило, мають пароксизмальну форму ФП, тоді як пацієнти зі структурною патологією серця мають схильність до більш тривалого перебігу ФП.
ФП сама по собі здатна спричинити прогресуючі зміни в електрофізіології передсердь, зокрема значне скорочення рефрактерного періоду, що у свою чергу сприяє продовженню аритмії. Клінічні дослідження свідчать про те, що у пацієнтів з часто рецидивуючою ФП з часом можуть розвиватися електрофізіологічні зміни, через які ФП може прогресувати до постійної форми. Більше того, тривалість епізоду ФП є потужним предиктором збереження синусового ритму після кардіоверсії: чим довже тривав епізод, тим вище ризик рецидиву ФП.
Класифікація
Відповідно до рекомендацій Європейського товариства кардіологів, розроблених у співробітництві з Європейською асоціацією з торакальної хірургії у 2020 році, на сьогоднішній день виділяють такі форми фібриляції передсердь:
- вперше виявлена (вперше діагностована);
- пароксизмальна;
- персистуюча;
- тривало персистуюча;
- постійна.
Вперше виявлена (вперше діагностована) ФП ‒ це епізод ФП, діагностований вперше в житті пацієнта, незалежно від клінічних симптомів або тривалості аритмії.
Пароксизмальна форма ‒ це епізод ФП, яка завершується спонтанно або в результаті медичного втручання впродовж 7 днів від початку.
Персистуюча форма ‒ це епізод ФП тривалістю більше 7 днів, включно з епізодами, перерваними в результаті медичного втручання (фармакологічна або електрична кардіоверсія) ≥ 7 днів від початку.
Тривало персистуюча форма – це епізод ФП тривалістю більше 12 місяців, у випадку обрання стратегії відновлення ритму.
Постійна форма ‒ це форма ФП, у відношенні якої пацієнтом та лікарем прийнято спільне рішення відмовитися від спроб відновити/підтримувати синусовий ритм. Це ключова відмінність постійної форми ФП від тривало персистуючої. У випадку перегляду стратегії на користь відновлення синусового ритму, постійна форма ФП має бути перейменована на тривало персистуючу ФП.
Формулюючи діагноз, окрім форми ФП, також доцільно вказувати ризик розвитку інсульту (з використанням шкали CHA2DS2-VASc), тяжкості симптомів ФП ( з використанням шкали EHRA), а також тяжкості субстрату, зокрема коморбідності, серцево-судинні фактори ризику.
Клінічна картина
Фібриляція передсердь у більшості випадків супроводжується появою у пацієнта відчуття серцебиття, перебоїв в роботі серця, задишки, дискомфорту в грудній клітці, головокружіння, зниження толерантності до фізичних навантажень.
У частини пацієнтів фібриляція супроводжується прискореним пульсом, болем у грудях та іншими симптомами, а у деяких протікає в прихованій формі й діагностується лише при розвитку інсульту або серцевої недостатності.
Ознаками фібриляції передсердь можуть бути:
- неритмічне серцебиття;
- швидкий пульс;
- біль у грудях;
- задишка;
- відчуття браку повітря;
- запаморочення;
- слабкість;
- втрата свідомості.
Найчастіше при миготливій аритмії пацієнт відчуває порушення серцевого ритму, підвищення частоти пульсу та задишку. Інші симптоми, як правило, з’являються при наявності інших хвороб серця – гіпертонії, стенокардії, серцевої недостатності тощо.
Для оцінки тяжкості клінічних проявів фібриляції передсердь використовується шкала EHRA.
| Симптоми | Опис | |
| 1 | відсутні | ФП не викликає симптомів |
| 2a | легкі | симптоми не порушують нормальної щоденної активності |
| 2b | помірні | симптоми не порушують нормальної щоденної активності, проте викликають неприємні відчуття у пацієнта |
| 3 | тяжкі | симптоми обмежують нормальну щоденну активність |
| 4 | симптоми, які роблять нормальне функціонування неможливим | симптоми унеможливлюють нормальне функціонування пацієнта |
Шість симптомів, у тому числі серцебиття, втома, запаморочення, задишка, біль у грудях і тривога під час ФП, оцінюються з огляду на те, як це впливає на щоденну активність пацієнта, починаючи від відсутності до частоти або тяжкості симптомів, які призводять до припинення повсякденної діяльності. Для вимірювання ефектів лікування анкети якості життя та симптомів мають бути чутливими до змін навантаження на ФП. Шкала симптомів EHRA – це інструмент лікаря для кількісної оцінки симптомів, пов’язаних із ФП, який використовується для прийняття рішень щодо лікування ФП, зумовлених симптомами, і був пов’язаний із несприятливими результатами у пацієнтів із більшою симптоматикою (оцінка 3–4) порівняно з пацієнтами з ФП з оцінкою 1–2. Однак він не враховує параметри симптомів, такі як тривога, занепокоєння щодо лікування та побічні ефекти ліків, які враховуються загальними шкалами якості життя, або результатами, пов’язані з симптомами, про які повідомляв пацієнт. Оскільки часто спостерігаються розбіжності між результатами, які повідомляють пацієнти, та результатами, оціненими лікарями, пов’язані з ФП рішення щодо лікування також повинні ґрунтуватися на кількісному сприйнятті пацієнтом симптомів, але необхідні подальші дослідження для визначення оптимального інструменту(ів) для збору цієї інформації.
Нерідко епізод ФП призводить до дестабілізації гемодинаміки, що може супроводжуватися втратою свідомості, симптомною гіпотензією, розвитком симптомів гострої серцевої недостатності, ішемії міокарда або навіть кардіогенного шоку.
Окрім можливої дестабілізації гемодинаміки, найбільшу загрозу для пацієнта з ФП становлять тромбоемболічні ускладнення, серед яких ішемічний інсульт займає провідне місце.
Утім нерідко фібриляція передсердь може протягом тривалого часу залишатися непоміченою через безсимптомний перебіг і діагностується випадково під час реєстрації ЕКГ.
Фізикальне обстеження
Головною об’єктивною ознакою ФП є нерегулярність серцевих тонів, яка виявляється під час фізикального обстеження, а саме аускультації серця. Частота серцевих скорочень варіює від нормальних значень до прискореного серцебиття. Важливою ознакою фібриляції передсердь також є дефіцит пульсу-різниця між частотою серцевих скорочень та частотою пульсу на променевій артерії. Артеріальний тиск у пацієнтів з ФП нерідко підвищений, хоча може бути нормальним або навіть зниженим у пацієнтів з ознаками дисфункції лівого шлуночка та падіння серцевого викиду на тлі тахісистолічної форми ФП.
Окрім цього, під час фізикального обстеження пацієнта треба звертати увагу на наявність у пацієнта ознак захворювання щитоподібної залози (екзофтальм, збільшення щитоподібної залози в розмірах), як однієї з можливих причин порушення ритму; ознак серцевої недостатності (вибухання яремних вен, хрипи в легенях, збільшення частоти дихальних рухів, додаткові 3 та 4 тони серця, набряки нижніх кінцівок), тромбоемболічних ускладнень (геміпарез, геміплегія, анізокорія) та інші.
Методи обстеження
Обов’язкові методи обстеження пацієнта з ФП включають:
- розгорнутий клінічний аналіз крові;
- біохімічний аналіз крові (оцінка функції нирок, визначення рівня електролітів);
- гормональне дослідження (оцінка функції щитоподібної залози);
- ЕКГ у 12 відведеннях;
- трансторакальне УЗД серця.
За окремими показаннями також можливе проведення додаткових методів обстеження, які включають:
- амбулаторний моніторинг ЕКГ (оцінка ефективності контролю частоти серцевих скорочень, виявлення пауз або брадикардії);
- трансезофагальне УЗД серця (для виявлення тромбу в лівому передсерді);
- електрофізіологічне дослідження та інші.
Більш детально за посиланням:
Диференційний діагноз
Фібриляцію передсердь необхідно диференціювати з:
- тріпотінням передсердь
- мультифокальною передсердною тахікардією
Для тріпотіння передсердь, як і для фібриляції передсердь, характерні скарги на серцебиття, перебої в роботі серця, що можуть асоціюватися з відчуттям дискомфорту чи болю в грудях, задишкою, відчуттям нестачі повітря, симптомною гіпотензією, головокружінням, втратою свідомості.
При фізикальному обстеженні пацієнта з тріпотінням пересердь часто виявляють прискорення ЧСС, хоча ЧСС може залишатися й нормальною. Якщо при фібриляції передсердь серцеві тони завжди нерегулярні, при тріпотінні передсердь серцеві тони можуть бути як нерегулярними, так і регулярними.
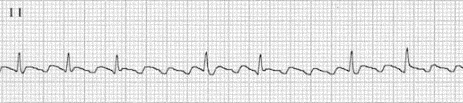
Остаточно диференціювати фібриляцію передсердь від тріпотіння передсердь допомагає ЕКГ. Для тріпотіння передсердь характерна, так звана, пилкоподібна ЕКГ з частотою передсердних скорочень від 350 до 450 уд./хв., у той час як при фібриляції передсердь частота передсерних скорочень складає від 450 до 650 уд./хв.
Рисунок 2. Тріпотіння передсердь. Зображення інтернет-ресурсу liftl.com
Для мультифокальної передсердної тахікардії, як і для фібриляції передсердь, характерні скарги на серцебиття, перебої в серці, які можуть супроводжуватися відчуттям дискомфорту чи болю в грудях, задишкою, відчуттям нестачі повітря, симптомною гіпотензією, головокружінням.
При фізикальному обстеженні пацієнта з мультифокальною передсердною тахікардією завжди виявляють прискорення ЧСС, хоча при ФП ЧСС інколи залишається нормальною. Як при фібриляції передсердь, так і при мультифокальній передсердній тахікардії серцеві тони завжди нерегулярні.
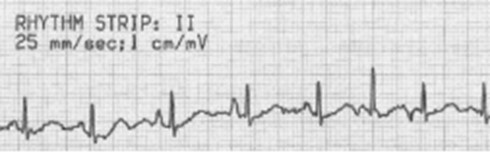
Остаточно диференціювати фібриляцію передсердь від мультифокальної передсердної тахікардії допомагає ЕКГ. Для мультифокальної передсердної тахікардії, як і для ФП, характерний нерегулярний серцевий ритм зі значним збільшенням частоти серцевих скорочень, але при мультифокальній передсердній тахікардії зубці Р збережені, хоча їх морфологія різна, у той час як при ФП зубці Р відсутні взагалі, а замість них присутня хвиля f.
Рисунок 3. Мультифокальна передсердна тахікардія. Зображення інтернет-ресурсу liftl.com
Лікування
Ключовими задачами в лікуванні пацієнтів з ФП є:
- попередження тромбоемболічних ускладнень;
- контроль симптомів;
- корекція факторів серцево-судинного ризику та супутніх захворювань.
Попередження тромбоемболічних ускладнень
Як зазначалося раніше, тромбоемболічні ускладнення (особливо ішемічний інсульт) представляють основну небезпеку у пацієнтів з ФП, тому попередження їх виникнення є однією з головних цілей лікування пацієнтів з ФП.
Для оцінки ризику тромбоемболічних ускладнень та визначення потреби у тривалій антикоагулянтній терапії у пацієнтів з ФП використовується шкала CHA2DS2-VASc.
Шкала CHA2DS2-VASc для оцінки ризику інсульту у пацієнтів з ФП
| Категорія | Бали | |
| C | Хронічна серцева недостатність | 1 |
| H | Гіпертензія (>140/90 мм рт ст) | 1 |
| A2 | Вік≥75 років | 2 |
| D | Цукровий діабет | 1 |
| S2 | Перенесений інсульт або ТІА | 2 |
| V | Судинне захворювання (ІМ, атеросклеротична бляшка, облітеруючий атеросклероз судин нижніх кінцівок та інші) | 1 |
| A | Вік 65-74 років | 1 |
| Sc | Жіноча стать | 1 |
Відповідно до рекомендацій Європейського товариства кардіологів (2020р):
- при сумі балів 0 у чоловіків та 1 у жінок ризик тромбоемболічних ускладнень вважається низьким, що не вимагає призначення антитромботичних препаратів;
- при сумі балів 1 у чоловіків та 2 у жінок призначення оральних антикоагулянтів можна розглянути в індивідуальному порядку після зваження усіх потенційних ризиків та користі;
- при сумі балів ≥2 у чоловіків та ≥3 у жінок ризик тромбоемболічних ускладнень вважається високим, рекомендоване призначення оральних антикоагулянтів.
Кожному пацієнту, якому показане призначення тривалої антитромботичної чи антикоагулянтної терапії, необхідно обов’язково проводити оцінку ризику геморагічних ускладнень за шкалою HAS-BLED з метою попередження їх виникнення.
Шкала HAS-BLED для оцінки ризику геморагічних ускладнень у пацієнтів з ФП
| Категорія | Бали | |
| H | Гіпертензія (>160 мм рт ст) | 1 |
| A | Печінкова або ниркова дисфункція | 1 за кожний |
| S | Інсульт | 1 |
| B | Кровотеча | 1 |
| L | Лабільне МНВ | 1 |
| E | Вік >65 років | 1 |
| D | Прийом ліків (НПЗП, інші антитромбоцитарні препарати) або алкоголю | 1 за кожний |
При сумі балів за шкалою HAS-BLED≥3 ризик геморагічних ускладнень вважається високим. Необхідно зауважити, що високий геморагічний ризик не може бути причиною для повної відмови від антикоагулянтів! В такому випадку рекомендовано запровадити заходи щодо корекції/усунення змінних факторів ризику кровотечі, посилити регулярний огляд та тривале спостереження за пацієнтом.
Утім, існують абсолютні протипоказання для призначення оральних антикоагулянтів, серед яких: активна кровотеча, тяжка тромбоцитопенія (менше 50*109/л), тяжка анемія, нещодавно перенесений внутрішньмозковий крововилив.
До оральних антикоагулянтів, які найчастіше призначають пацієнтам з ФП, відносяться:
Антагоніст вітаміну К (варфарин) блокує каскад активації згортальної системи крові за рахунок пригнічення карбоксилювання II, VII, IX та X факторів коагуляції. Враховуючи високу варіабельність концентрації варфарину, зумовлену генетично-обумовленими особливостями його метаболізму, взаємодією з іншими препаратами, харчовими продуктами, підбір необхідної дози препарату вимагає поступової титрації з регулярним визначенням МНО. Ознайомитися з алгоритмом призначення та підбору ефективної дози варфарину можна за посиланням https://clincasequest.academy/warfarin/
Прямі інгібітори фактора Ха (рівароксабан, апіксабан, едоксабан) інактивують фактор Ха, необхідний для активації тромбіну. Беззаперечними перевагами нових оральних антикоагулянтів (НОАК) порівняно з варфарином є швидкий початок дії, відсутність необхідності титрування дози, низький ризик кровотеч, відсутність необхідності лабораторного моніторингу ефективності та безпечності. Утім, необхідно нагадати, що дозування препаратів залежить від функції нирок пацієнта. Ознайомитися з рекомендаціями щодо призначення ефективної дози НОАК можна за посиланням https://clincasequest.academy/anticoagulant-dose/
Прямий інгібітор тромбіну (дабігатран) попереджує перетворення фібриногену у фібрин, безпосередньо інактивуючи тромбін. Враховуючи переважну екскрецію дабігатрану нирками (80%), перед призначенням препарату треба пересвідчитися, що кліренс креатиніну вищий за 30 мл/хвилину.
У разі виникнення кровотеч на тлі прийому оральних антикоагулянтів у пацієнтів з ФП, дійте за алгоритмом, представленим за посиланням https://clincasequest.academy/noac-bleeding/
У разі гострої потреби у проведенні оперативного лікування пацієнту з ФП, який приймає антикоагулянту терапію, керуйтесь алгоритмом, представленим за посиланням https://clincasequest.academy/anticoagulant_therapy/
Нові оральні антикоагулянти
| Дабігатран | Рівароксабан | Апіксабан | Едоксабан | |
| Стандартна доза | 150 мг 2 рази на день | 20 мг 1 раз на день | 5 мг 2 рази на день | 60 мг 1 раз на день |
| Редукована доза | 110 мг 2 рази на день | 15 мг 1 раз на день | 2,5 мг 2 рази на день | 30 мг 1 раз на день |
| Критерії редукції дози | вік≥80 років; одночасний прийом верапамілу; підвищений геморагічний ризик | ШКФ 15-49 мл/хв | вік≥80 років; маса тіла≤60 кг або креатинін≥133 мкмоль/л | ШКФ 15-50 мл/хв.; маса тіла≤60 кг або одночасний прийом дронедарону, циклоспорину, еритроміцину або кетоконазолу |
Інші антитромботичні препарати, такі як аспірин та клопідогрель продемонстрували меншу ефективність, ніж варфарин, у зниженні ризику тромбоемболічних ускладнень, при однаковому геморагічного ризику.
Контроль симптомів
Контроль симптомів ФП досягається завдяки контролю частоти шлуночкових скорочень або ритму серця.
Стратегія відновлення синусового ритму
Стратегія відновлення синусового ритму (кардіоверсія) показана симптомним пацієнтам (особливо пацієнтам з тяжкими симптомами або скомпрометованою гемодинамікою) з метою зменшення клінічних проявів аритмії та покращення якості життя. Кардіоверсії завжди має передувати антикоагулянтна терапія!
Окрім цього, кардіоверсія має переваги у пацієнтів молодого віку; при першому епізоді ФП; розвитку кардіоміопатії, зумовленої тахікардією; при нормальному або незначно зміненому лівому передсердю; за відсутності або за незначної супутньої патології; при неможливості адекватного контролю частоти серцевих скорочень; якщо епізод ФП був викликаний якимось гострим станом (наприклад, пневмонія, вживання алкоголю, електролітні порушення); при наявності бажання у пацієнта.
Основними методами відновлення синусового ритму є електрична та фармакологічна кардіоверсія.
Невідкладна електрична кардіоверсія показана при:
- епізоді ФП з високою частотою шлуночкових скорочень (ЧСС>250 уд/хв), на тлі гострого інфаркту міокарда, нестабільної стенокардії;
- епізоді ФП, який супроводжується симптомною гіпотензією, гострою або прогресуючою хронічною серцевою недостатністю;
- тяжкому епізоді ФП, який не піддається медикаментозному лікуванню.
Планова електрична кардіоверсія показана при:
- неефективності медикаментозної терапії;
- непереносимості антиаритмічних препаратів або ризику, пов’язаному з їх призначенням;
- прогресуванні серцевої недостатності, погіршенні адекватної перфузії серця, мозку, нижніх кінцівок, пов’язаному з тахіаритмією;
- вказання в анамнезі електричної кардіоверсії як єдиного ефективного методу лікування аритмії у пацієнта.
У інших випадках можливе застосування фармакологічної кардіоверсії з використанням антиаритмічних препаратів, вказаних нижче.
| Препарати | Дозування | Протипоказання |
| Аміодарон | 5-7 мг/кг в/в впродовж 1-2 год, з наступним в/в введенням 50 мг/год (максимум 1,2г впродовж 24 год) | Застосовується з обережністю при одночасному прийомі препаратів, що подовжують інтервал QT. |
| Флекаінід | 200-300 мг перорально або 2 мг/кг в/в впродовж 10 хв | Не використовується при структурній патології серця та/або ішемічній хворобі серця, при подовженому інтервалі QT, при ураженнях провідної системи серця. |
| Пропафенон | 450-600 мг перорально або 1,5-2,0 мг/кг в/в впродовж 10 хв | Протипоказаний при ІХС, при серцевій недостатності зі зниженою фракцією викиду лівого шлуночка, при подовженому інтервалі QT, при синдромі Бругада, при значній гіпотензії, при ураженнях провідної системи серця. |
| Ібутилід | 1 мг в/в впродовж 10 хв (0,01 мг/кг при вазі тіла˂60 кг) | Протипоказаний при подовженому інтервалі QT |
Вибір оптимального антиаритмічного препарату залежить перш за все від його безпечності у конкретного пацієнта:
- у пацієнтів без структурної патології серця можливе використання будь-якого з перелічених вище антиаритмічних препаратів (безумовно, за відсутності протипоказань);
- у пацієнтів зі структурною патологією серця (гіпертрофія, ішемія, застійна серцева недостатність) препаратом вибору в Україні є аміодарон.
Для запобігання рецидивам ФП після відновлення синусового ритму рекомендовано використовувати такі препарати: аміодарон, дронедарон, флекаінід, пропафенон, соталол, дизопірамід. Окрім вищезазначених антиаритмічних препаратів, існують і інші препарати з антиаритмічними властивостями, такі як іАПФ, БРАII, антагоністи мінералокортикоідних рецепторів, бета-блокатори, статини.
Підхід “таблетка в кишені”
В окремих пацієнтів з ФП, епізод якої розпочався нещодавно, за відсутності значущої структурної патології серця та відсутності нестабільності гемодинаміки, можливий самостійний однократний пероральний прийом високої дози пропафенону для відновлення синусового ритму. Утім, необхідно зауважити, що попередньо необхідно пересвідчитися у безпечності такого лікування (наприклад, якщо пропафенон успішно використовувався в якості антиаритміка під час перебування пацієнта в умовах стаціонару).
Стратегія контролю частоти серцевих скорочень
Стратегія контролю частоти скорочень показана:
- в якості фонової терапії усім пацієнтам з ФП;
- безсимптомним пацієнтам або пацієнтам з мінімальними симптомами ФП;
- пацієнтам в разі неефективності терапії з відновлення синусового ритму;
- пацієнтам, якщо ризики відновлення синусового ритму переважають користь.
Інтенсивність зниження частоти серцевих скорочень у пацієнта з ФП залежить від клінічної симптоматики. У безсимптомних пацієнтів або у пацієнтів з нетяжкими симптомами ФП можливий більш гнучкий контроль ЧСС (зниження та утримання ЧСС на рівні ˂110 уд/хв. у стані спокою). Якщо пацієнт залишається симптомним, ЧСС має бути знижена до такого рівня, при якому симптоми аритмії зникнуть або будуть легко переноситися пацієнтом.
У пацієнтів з тяжкими симптомами застосовується стратегія жорсткого контролю ЧСС (цільова ЧСС˂80 уд/хв. у стані спокою та ˂110 уд/хв. при фізичному навантаженні), для оцінки безпечності такого підходу слід провести добове амбулаторне моніторування ЕКГ для виявлення пауз та брадикардії.
| Препарати | В/в ведення | Підтримуюча доза | Протипоказання |
| Бета-блокатори | |||
| Метопрололу тартрат | 2,5-5 мг в/в болюсно | 25-100 мг 2 рази на день | Бета-блокатори протипоказані при гострій серцевій недостатності; бронхоспазмі в анамнезі; при бронхіальній астмі використовуйте бета1-блокатори |
| Метопрололу сукцинат | – | 50-400 мг 1 раз на день | |
| Бісопролол | – | 1,25-20 мг 1 раз на день | |
| Атенолол | – | 25-100 мг 1 раз на день | |
| Есмолол | 500 мкг/кг в/в болісно впродовж 1 хв., з наступним введенням 50-300 мкг/кг/хв. | – | |
| Небіволол | – | 2,5-10 мг 1 раз на день | |
| Карведілол | – | 3,125-50 мг 2 рази на день | |
| Антагоністи кальцієвих каналів | |||
| Верапаміл | 2,5-10 мг в/в болісно впродовж 5 хв. | 40 мг 2 рази на день до 480 мг (з пролонгованим вивільненням) 1 раз на день | Протипоказані при серцевій недостатності зі зниженою фракцією викиду |
| Дилтіазем | 0,25 мг/кг в/в болісно впродовж 5 хв., потім 5-15 мг/год | 60 мг 3 рази на день до 360 мг (з пролонгованим вивільненням) 1 раз на день | |
| Серцеві глікозиди | |||
| Дігоксин | 0,5 мг в/в болюсно | 0,0625-0,25 мг 1 раз на день | Перевірте функцію нирок перед початком терапії, при зниженій функції нирок доза має бути скоригована |
| Інші препарати | |||
| Аміодарон | 300 мг, попередньо розчинивши у 200 мл 5% глюкози в/в крапельно впродовж 30-60 хв. | 200 мг 3 рази на день впродовж 4 тижнів з наступним зниженням дози до 200 мг 1 раз на день | Протипоказаний при патології щитоподібної залози |
Корекція факторів серцево-судинного ризику та супутніх захворювань
Фактори серцево-судинного ризику та супутня патологія значно впливають на ризик розвитку ФП. Раніше ми вже зазначали, які саме фактори ризику та яка саме коморбідна патологія можуть спричинити пароксизм ФП.
До необхідних заходів щодо корекції способу життя відносять: корекція маси тіла, обмеження вживання алкоголю, обмеження надмірних фізичних навантажень та дотримання достатньої фізичної активності, суворий контроль АТ (≤130/80 мм рт. ст.), оптимальний глікемічний контроль, покращення нічного сну для запобігання епізодів апное.
Читайте також:
Зареєструйтеся на нашому сайті прямо зараз, щоб мати доступ до більшої кількості навчальних матеріалів!
Підписатися на наші сторінки:
Література
- 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association of Cardio-Thoracic Surgery (EACTS): The task force for the diagnosis and management of atrial fibrillation of the European Society of Cardiology (ESC) developed with the special contribution of the European Heart Rhythm Association (EHRA) of the ESC. European Heat Journal (2020), 42(5), 373−498. doi: 10.1093/eurheartj/ehaa612
- 2019 AHA/ACC/HRS Focused Update of the 2014 AHA/ACC/HRS Guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/ American Heart Association Task force on clinical practice guidelines and the Heart Rhythm Society in collaboration with the Society of Thoracic Surgeons. Circulation. 2019; 140:e125−e151. doi.org/10.1161/CIR.0000000000000665
- 2021 NICE guideline on Atrial fibrillation: diagnosis and management. https://www.nice.org.uk/guidance/ng196
- Markides V, Schilling RJ. Atrial fibrillation: classification, pathophysiology, mechanisms and drug treatment. Heart. 2003; 89: 939-943.
- Наказ МОЗ України №597 від 15.06.2016 “Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги при фібриляції передсердь”.
Консультація пацієнта із спонтанною дисекцією коронарних судин – рекомендації ОСКІ
Автори: Hanna Samoilova, Nataliia Lopina Початок консультації Вимийте руки та при необхідності надіньте ЗІЗ (засоби…
Cимптомна брадикардія
Симптомна брадикардія виникає при зниженні частоти серцевих скорочень менше 50 ударів за хвилину. Найчастіше в…
Шлуночкові тахікардії
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров Клінічна термінологія Шлуночкову тахікардію визначають як три або…
Тромбоемболія легеневої артерії
Тромбоемболія легеневої артерії (ТЕЛА) ‒ це загрозливе для життя захворювання, обумовлене оклюзією стовбура чи гілок…
Проведення експрес тесту на визначення маркерів некрозу міокарду
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров У пацієнтів з ГКС може буде позитивний експрес-тест…
Гострий коронарний синдром без елевації сегменту ST
Автори: Т.Д. Данілевич, А.В. Зінченко, А.А. Сідоров Визначення Гострий коронарний синдром – це група симптомів…