Рекомендації щодо ведення жінок з інфарктом міокарда, пов’язаним з вагітністю

Хоча гострий інфаркт міокарда ускладнює вагітність відносно рідко, не більше ніж 6 випадків на 100 000 пологів, ішемічна хвороба серця є причиною 20% усіх материнських серцевих смертей. Рівень смертності в останніх сучасних дослідженнях оцінюється в 5 до 12 % і є вищим, ніж рівень смертності від інфаркту серед невагітних жінок репродуктивного віку [1,2]. В останньому дослідженні «Реєстру вагітності та серцевих захворювань (ROPAC)» ішемічна хвороба серця становила < 2% від усіх захворювань серця у матері[3,4,5].
Мета-аналіз популяційних міжнародних досліджень виявив, що захворюваність на інфаркт міокарда, пов’язаний з вагітністю (Pregnancy-associated myocardial infarction (PAMI)) є найвищою в допологовий період. У 150 звітах про випадки інфаркту у жінок, 24 % були діагностовані в третьому триместрі, а у 47% – після пологів. Більшість (75%) мали інфаркт міокарда з підйомом сегмента SТ, а 24% мали серйозне зниження фракції викиду лівого шлуночка меншу ніж 30%, з кардіогенними ускладненнями – шоком (38%) та шлуночковими аритміями (12%). В іншому дослідженні у жінок з інфарктом внаслідок диссекції коронарної артерії – 54% виникли протягом першого тижня після пологів [6,7].
Етіологія
Вагітність пов’язана зі збільшенням ризику гострого інфаркту міокарда у 3-4 рази порівняно з невагітними жінками відповідного віку. Поряд з класичними факторами ризику, такими як куріння, вік матері, гіпертонія, діабет, ожиріння та дисліпідемія, тут приєднуються додаткові фактори. Це (пре)еклампсія, тромбофілія, переливання крові, післяпологова інфекція, багатоплідність та післяпологова кровотеча. Зростання материнської смертності пояснюється збільшенням кількості жінок похилого віку, які вагітніють, наявними супутніми захворюваннями, такими як цукровий діабет і гіпертонія, а також зростанням числа жінок із вродженими вадами серця, які доживають до дітородного віку [8].
Одним із найбільш постійно зареєстрованих факторів ризику інфаркту асоційованого з вагітністю є вік більше 35 років. У жінок старших за 40 років ризик гострого інфаркту міокарда зростає на 20% у порівнянні з молодшою віковою групою. Клініцисти повинні залишатися підозрілими щодо інфаркту міокарда у жінок після пологів із болем у грудях або гострою задишкою, а також у тих із зупинкою серця, навіть за відсутності електрокардіографічних змін [9]. У дослідженні CARPREG II (Cardiac Disease in Pregnancy) відзначено приблизно 5-7% ризик несприятливих серцевих подій у жінок з ішемічною хворобою серця в анамнезі [10].
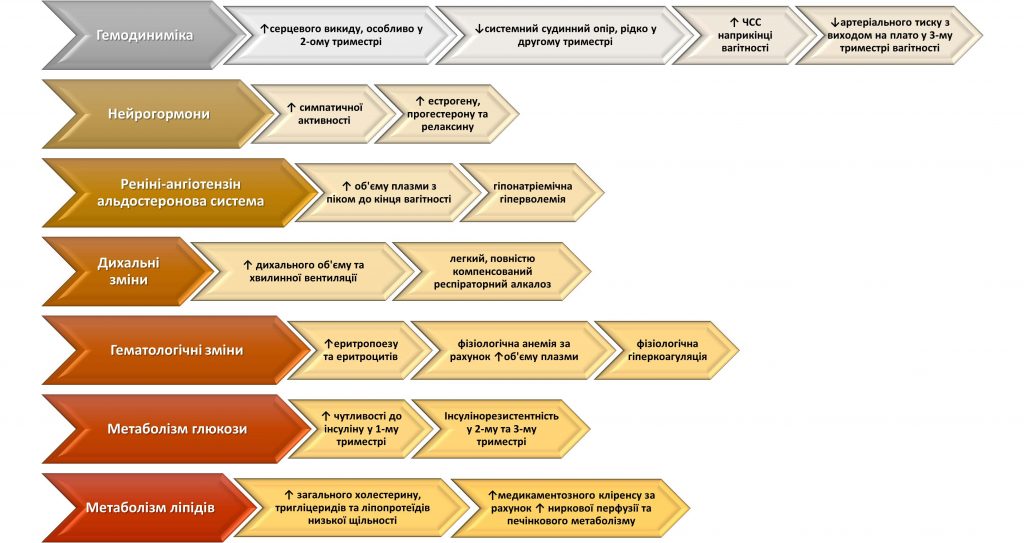
Етіологія гострого коронарного синдрому під час вагітності відрізняється від загальної сукупності і у більшості випадків має неатеросклеротичний характер. Механізми розвитку гострого коронарного синдрому, пов’язані з вагітністю та полягають у спонтанному розшаруванні стінки коронарної артерії, спазмі ангіографічно нормальних коронарних артерій і формуванні коронарного тромбозу. Гострий інфаркт міокарда, пов’язаний з розшаруванням стінки коронарної артерії, найчастіше виникає на пізніх/ранніх термінах вагітності, під впливом коливання рівню естрогену/прогестерону, після пологів і переважно залучає ліву коронарну судину. Механізми інфаркту міокарда при ангіографічно нормальному коронарному руслі залишаються неясними і, вірогідно, пов’язаний з транзиторним коронарним спазмом. Коронарний тромбоз при відсутності атеросклерозу розвивається через гіперкоагуляцію і може бути результатом парадоксальної емболізації (рисунок 1). [6]
Рисунок 1. Гемодинамічні, фізіологічні та метаболічні зміни на тлі вагітності. *Серцевий викид, частота серцевих скорочень і артеріальний тиск значно збільшуються під час пологів. ЧСС – частота черцевих скорочень.
Причини гострого інфаркта міокарда у вагітних
Як обструктивні, так і необструктивні ураження коронарних артерій можуть спричинити гострий інфаркт на тлі вагітності. Пацієнти з інфарктом з нормальними або необструктивними (<50% стенозу) коронарними артеріями вважаються такими, що мають інфаркт міокарда з необструктивними коронарними артеріями. Причини інфаркту з необструктивними коронарними артеріями включають руйнування коронарної бляшки з тромбозом і спонтанним тромболізисом; коронарний вазоспазм з розрішенням перед ангіографією; коронарна емболія; спонтанна дисекція коронарної артерії; і мікросудинна дисфункція.
- Розрив або ерозія бляшки з атеротромбозом
Обструктивна нестабільна атеросклеротична ішемічна хвороба коронарних артерій є основним механізмом приблизно однієї третини всіх інфарктів при вагітності. Це відбувається внаслідок розриву тонкої фіброзної оболонки багатої на ліпопротеїни, бляшки з оголенням некротичного ядра та утворенням коронарного тромбозу. Коронарний тромб також може утворюватися у відповідь на ерозію бляшки, у якій порушений ендотелій екстрагується, створює бляшку, яка переважно складається з гладком’язових клітин і протеогліканів. Механізм не відрізняється від такового у невігітних жінок чи у чоловічій популяції.
- Спонтанна дисекція коронарної артерії
Хоча точна поширеність невизначена, все частіше визнається, що спонтанна дисекція коронарної артерії може спричинити принаймні одну третину інфарктів на фоні вагітності. Спонтанна дисекція коронарної артерії є наслідком гематоми з або без розриву інтими коронарних артерій, пов’язаної з обструкцією кровотоку, яка не пов’язана з атеросклеротичними, ятрогенними або травматичними причинами. Внутрішньокоронарний тромб зазвичай відсутній. Пацієнти зі спонтанною дисекцією коронарної артерії зазвичай мають фіброзно-м’язову дисплазію або інші артеріопатії, такі як дилатація, дисекція та аневризми [23].
Жінки зі спонтанною дисекцією коронарної артерії, асоційованою з вагітністю, часто мають більш важкий перебіг, включаючи гемодинамічну нестабільність і багатосудинну дисекцію. Що стосується факторів ризику, то такі жінки частіше мають анамнез терапії щодо безпліддя, багатоплідності та прееклампсії. Частота рецидивів дисекції становить приблизно 15%, тому слід з обережністю відноситися до планування подальших вагітностей. Враховуючи непередбачуваний характер цього стану, рекомендації щодо стратифікації ризику під час вагітності нечіткі [3, 21].
- «In-situ» тромбоз або емболія
Вагітність – це фізіологічний стан гіперкоагуляції, який може призвести до внутрішньокоронарного тромбу або емболії коронарних артерій «in-situ». До сприятливих станів належать хвороба Кавасакі, системні запальні стани та аутоімунні розлади, такі як синдром антифосфоліпідних антитіл, пухлини, злоякісні пухлини, фібриляція передсердь, кардіоміопатія та захворювання клапанів серця. Оскільки половина пацієнток із тромбозом під час вагітності має супутню тромбофілію, а тромбофілія є фактором ризику, тому рекомендовано тестування на тромбофілію, якщо немає іншої схильності до тромбозу після вагітності.
- Коронарний вазоспазм
Коронарний вазоспазм важко діагностувати, але спостерігалося, що він спричиняє гострий інфаркт міокарду з підйомом ST під час вагітності і був відзначений у 2% випадків інфарктів на тлі вагітності. Тривалий вазоспазм може сприяти утворенню внутрішньокоронарного тромбу.
Начастіші причини гострого коронарного синдрома представлені на рисунку 2 [11].
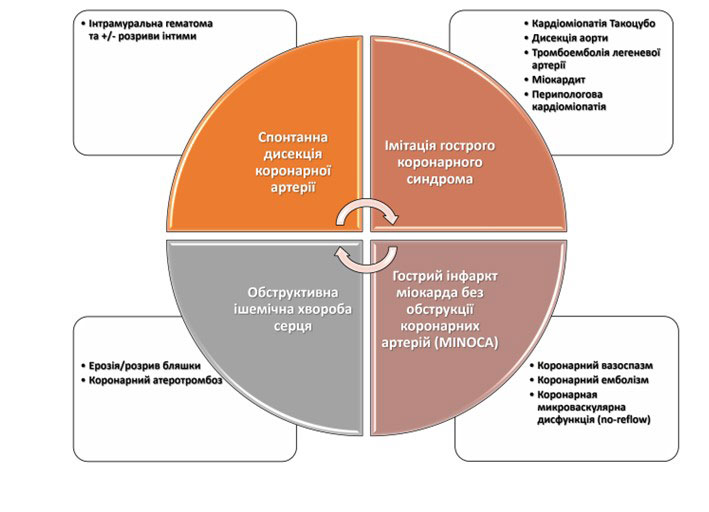
Рисунок 2. Основні причини гострого коронарного синдрому у вагітних жінок.
Діагностика
Діагноз інфаркту міокарда, асоційованого з вагітністю, ставиться, коли гострий інфаркт міокарда з підйомом сегмента ST або без підйома виникає під час вагітності або протягом 6–12 тижнів після пологів.
Гострий інфаркт міокарда з підйомом сегмента ST визначається як елевація сегмента ST або блокада лівої ніжки пучка Гіса на ЕКГ із ознаками ураження міокарда, тобто підвищення рівня тропоніну. Гострий інфаркт міокарда з підйомом сегмента ST майже завжди являє собою повну гостру оклюзію коронарної артерії і, як результат, розвиток трансмурального інфаркту (включаючи всі шари стінки лівого шлуночка).
Гострий інфаркт міокарда без підйомом сегмента ST присутній, коли є підвищення тропоніну, але немає підйому сегмента ST на ЕКГ. Депресія сегмента ST або інверсія зубця Т можуть бути або не бути присутніми і не є обов’язковими діагностичними крітеріями. Патологічно гострий інфаркт міокарда без підйомом сегмента ST часто являє собою субтотальну оклюзію коронарної артерії, що призводить до менш серйозного пошкодження (субендокардіального).
Нестабільна стенокардія характеризується болем у грудях без підвищення рівня тропоніну. Нестабільна стенокардія позначається як така, що може призводити до розвитку більш важких форм інфаркту міокарда.
Стабільна стенокардія розглядається окремо від гострого коронарного синдрому, визначається як біль у грудях, який виникає під час стресу та полегшується під час відпочинку або прийому нітрогліцерину. Стенокардія, зокрема, відноситься до хронічного коронарного синдрому, лікування якого в основному включає консервативні заходи, такі як зміна способу життя та прийом антиангінальних препаратів (наприклад, бета-блокаторів або блокаторів кальцієвих каналів).
Інфаркт міокарда слід запідозрити у вагітних або породіль із зупинкою серця, гострим початком стенокардії або задишки, ішемічними змінами на ЕКГ або підвищенням серцевих біомаркерів. Cимптоми, дані об’єктивного огляду, ЕКГ та біомаркерів можуть виникати під час нормальної вагітності і їх важливо відрізняти від тих, що вказують на інфаркт (таблиця 1). Наприклад, задишка є поширеною на пізніх термінах вагітності, але задишка, пов’язана з ортопное або дискомфортом у грудній клітці, має спонукати до оцінки серцево-судинної системи. Нормальна вагітність може бути пов’язана з відхиленнями ЕКГ, включаючи відхилення осі вліво, появою зубців Q в нижній стінці і інверсією зубців T. Транзиторна депресія ST може виникнути у здорових жінок під час кесаревого розтину під регіонарною анестезією. Враховуючи це, інтерпретація ЕКГ може бути ускладнена, крім того, введення в анестезію при кесаревому розтині також може бути пов’язаним з депресією сегмента ST. Підвищення тропоніну в сироватці крові свідчить про ішемію міокарда, навіть при прееклампсії. Якщо ЕКГ не є діагностично значимою, вона може бути корисною. Диференціальна діагностика потребує виключення тромбоемболії легеневої артерії, розшарування аорти і прееклампсії. Потенційні ускладнення включають серцеву недостатність та кардіогенний шок (38%), аритмії (12%), рецидивуючу стенокардію (20%), материнську смертність (7%) і смерть плоду (7%) [6].
Таблиця 1. Нормальні та патологічні симптоми, обстеження та тестування під час вагітності та пологів.
| Нормальні зміни серцево-судинної системи на тлі вагітності та пологів | Патологічні зміни серцево-судинної системи на тлі вагітності та пологів | |
| Симптоми | Задишка, особливо у 3-му триместріЗниження толерантності до фізичного навантаження, серцебиття, легке головокружіння | Біль у грудях, стиснення, дискомфортЗадишка, особливо коли погіршується чи виникає раптовоІрадіація болі в руку, плече, щелепу, потужне потовиделення, нудота, блювання |
| Фізикальне обстеження | Нормальна або легка пульсація яремної вениМ’який, середньо-систолічний шумШироке розшеплення тону S3 та гучний тон S1Шийний венозний шум | Виражене розширення яремної вениГолосистолічний шум на верхівціДіастолічний шумФіксоване раздвоення тонів S2, S4Легеневі хріпи |
| Електрокардіограма | Зубець Q у відведенні III та aVFІнверсія зубця Т в відведенні III, V1-3Транзіторна депресія сегменту ST за умови проведення кесарева розтину | ST сегмент елеваціяСтійка депресія сегмента ST чи та, що з’явилася на фоні болюГлибока інверсія зубця Т чи у відвіденнях відмінних від V1-V3 |
| Серцеві біомаркери | Рівні піднімаються протягом 24 годин після пологівКреатинфосфокіназа та її МВ фракція зростає вдвічі після пологів та може привищити верхню межуПідвищення високочутливого тропоніну після неускладнених пологів у незначної кількості жінокПрееклампсія та гестаційна гіпертензія може призводити до підвищення рівню тропоніну | Підвищення біомаркерів на тлі появі нових симптомів, особливо, якщо вони не виникають одразу після пологівЯкщо підвищення більш ніж помірне або якщо рівень підвищується під час серійних вимірювань |
У таблиці 2 представлено рекомендації щодо ведення вагітних жінок з підозрою на гострий інфакрт міокарда та клас їх доказовості.
Таблиця 2. Загальні рекомендації менеджменту вагітної жінки з біллю в грудній клітці.
| Рекомендації | Клас | Рівень доказовості |
| ЕКГ та вимірювання рівня тропоніну рекомендовані вагітним жінкам, які мають біль у грудях | I | C |
| Рекомендується первинна коронарна ангіопластика як краща реперфузійна терапія для ГІМп ST під час вагітності. | I | C |
| Інвазивна стратегія лікування розглядається для хворих на ГІМ без підйома сегмента ST з високим ризиком ускладнень. | IIa | C |
| Слід розглянути можливість консервативного лікування для стабільних хворих на ГІМ без підйома сегмента ST з низьким ризиком ускладнень. | IIa | C |
| Необхідно розглянути можливість подальшого спостереження щонайменше протягом наступних 3 місяців. | IIa | C |
| Матерям не рекомендується годувати грудьми, якщо приймають антиагреганти, крім низькодозового аспірину через відсутність даних. | III | C |
Визначення серцевого ризику у вагітних із захворюванням серця вимагає інтеграції оцінок ризику, індивідуальних факторів і клінічного судження. Червоні стрілки показують змінні в оцінці ризику CARPREG II, яка використовується для прогнозування несприятливих серцевих подій у вагітних із захворюванням серця. Окрім змінних у шкалі ризику CARPREG II, можуть існувати інші фактори, які впливають на прогноз окремого пацієнта. Синя стрілка показує деякі інші змінні, які слід враховувати при оцінці ризиків вагітності, рисунок 3 [10].
Рисунок 3. Прогнозування настання несприятливих подій у вагітних жінок з наявними захворюваннями серцево-судинної системи
Диференційна діагностика
Низка серйозних станів може мати подібну клінічну картину, як гострий інфаркт міокарда у вагітних, іноді з аномальною ЕКГ та підвищенням біомаркерів некрозу міокарду (рисунок 4) [6,22].
Рисунок 4. Диференціальна діагностика інфаркту міокарда, асоційованого з вагітністю.
Як і у невагітних жінок, інфаркт міокарда, що асоційований з вагітністю діагностується, коли у відповідних клінічних умовах зустрічаються наведені вище визначення гострого інфаркту з підйомом та без підйому сегмента ST. Основними симптомами є біль у грудній клітці та задишка (Таблиця 3).
Таблиця 3. Діагностичні методи
| Особливості | |
| Симптоми | Загрудинний біль, задишка |
| Електрокардіограма | Депресія або елевація сегмента ST Інверсія зубця Т Втрата зубця R Новий зубець Q |
| Біомаркери | Підвищення тропоніну Т/І |
| Ехокардіографія | Зниження кінетики стінки лівого шлуночка |
Серцевий тропонін все ще є найкращим біомаркером для діагностики гострого інфаркту міокарда. Загалом, рівень тропоніну не змінюється під час нормальної вагітності. Помірне підвищення рівня серцевого тропоніну може спостерігатися у жінок з гіпертонічною хворобою та осіб з прееклампсією. Краще використовувати високочутливий тропонін для більш точної та швидкої діагностики гострого інфаркту.
Слід зазначити, що незначні електрокардіографічні зміни, що стосуються сегмента ST і зубця Т, були зареєстровані у здорових вагітних жінок під час пологів.
Ехокардіограма є дуже корисним інструментом, безпечним для діагностики вагітних пацієнток із болем у грудях або підозрою на гострий інфаркт. Майже всі пацієнти з гострим інфарктом демонструють аномалії руху стінки. Однак, ехокардіографія не є стандартним методом діагностики гострого інфаркту і часто цей метод виконується вже після стентування з метою оцінки раннього ремоделювання лівого шлуночка.
Навантажувальні тести з ЕКГ або без можна використовувати під час вагітності для діагностики індукованої ішемії після виключення інфаркту міркарду і коли гемодинамічний стан пацієнтки стабільний. Використання субмаксимального тесту (70% від максимальної прогнозованої частоти серцевих скорочень) рекомендовано через попередні повідомлення про брадикардію плода та зниження варіабельності серцевого ритму плоду під час помірних та важких фізичних навантажень матері.
Комп’ютерна коронарна томографія може бути корисною для виключення гострого коронарного синдрому в сумнівних випадках, але вона несе в собі ризик радіаційного опромінення та має нижчу чутливість до уражень малих дистальних судин. Крім того, для оптимальної візуалізації коронарного дерева можуть знадобитися високі дози бета-блокаторів для зниження ЧСС [12].
Лікування
Оперативна діагностика та лікування гострого інфаркту міокарда у вагітних є надзвичайно важливими через високу материнську та смерть плоду.
Смертність найвища серед жінок, які перенесли інфаркт міокарда під час госпіталізації з приводу пологів.
Відповідна терапія, зосереджена на покращенні стану матері, також збільшить виживаність плоду, і, отже, стан матері повинен диктувати клінічне лікування. Мультидисциплінарна кардіологічна група для вагітних може бути важливою для прийняття колективних рішень. До складу такої команди входять фахівці з кардіології, акушерства або медицини матері та плоду, анестезіології та, залежно від клінічної ситуації, кардіоторакальні хірурги, неонатологи та лікарі відділення інтенсивної терапії.
Лікування гострого інфаркту міокарда під час вагітності подібне до лікування в загальній популяції, включаючи методи реваскуляризації. Ангіографія є золотим стандартом діагностики ішемічної хвороби серця під час вагітності. При спонтанній дисcекції за умови застосування реваскуляризації слід враховувати вразливість судин з огляду на дуже високий ризик виникнення додаткової ятрогенної дисекції коронарних судин. Ведення такої пацієнтки має бути багатодисциплінарним, включаючи невідкладну, акушерську та серцево-судинну бригади, реваскуляризацію повинен проводити найдосвідченіший персонал через супутні ризики, пов’язані з коронарним втручанням у цій групі пацієнтів. При кардіогенному шоці слід застосовувати засоби для екстреної механічної підтримки кровообігу [13,14].
Фармакотерапія
Важливо, що стандарти лікування невагітної жінки з інфарктом міокарду мають бути стандартом для ліквання і вагітної жінки із деякими модифікаціями. Це включає використання аспірину, гепарину, клопідогрелю та нітратів. Повну дозу аспірину (325 мг) можна використовувати до 32 тижнія вагітності, а 81 мг можна використовувати у будь-який час під час вагітності. Гепарин є кращим антикоагулянтом, оскільки він не проникає крізь плаценту, і безпека його застосування під час вагітності встановлена.
Існує мало інформації щодо безпеки для плоду рекомендованої лікарської терапії при гострому інфаркті міокарда. Мабуть, низькі дози аспірину будуть безпечним, але інформації щодо інгібіторів P2Y12 недостатньо. Клопідогрель є інгібітором P2Y12, якому надають перевагу під час вагітності, і більш потужних інгібіторів P2Y12 слід уникати або використовувати з обережністю. Клопідогрель слід застосовувати лише за гострої необхідності та найкоротшим курсом. Можуть бути розглянуті монопрепарати аспірину, наприклад, при інфаркті, що спровокувала спонтанна дисекція коронарної артерії, хоча це ґрунтується на консенсусі експертів, і даних, що демонструють користь проти шкоди, бракує. За відсутності даних щодо використання інгібіторів глікопротеїну IIb/IIIa, їх використання не рекомендується, бівалірудину, прасугрелю та тикагрелору також. Подвійна антиагрегантна терапія (ПАТТ) доцільна, якщо планується черезшкірне коронарне втручання (ЧКВ) з внутрішньокоронарним стентуванням.
Бета-блокада можуть бути корисними для зменшення зсуву стресу при диссекції коронарної артерії. Бета-блокатори, як правило, вважаються безпечними під час вагітності, але використання інгібіторів ангіотензинперетворювального ферменту та блокаторів рецепторів ангіотензину слід відкласти після пологів через ризики для плоду. Рекомбінантний тканинний активатор плазміногену не проникає через плаценту, але може спричинити ускладнення у вигляді кровотечі (субплацентарна кровотеча). Фібринолітична терапія, якщо її можна провести своєчасно може бути особливо вірною стратегією для вагітних жінок, враховуючи численні причини ІМ, підвищений ризик кровотечі та відносні протипоказання до проведення фібринолітичної терапії. Тим не менш, повідомлялося про успішне використання тромболітиків під час вагітності, особливо для лікування емболії легеневої артерії [15].
Переваги короткочасної гепаринізації під час чрезщкірного коронарного втручання, ймовірно, переважають ризик кровотеч. Гепарин є кращим антикоагулянтом, оскільки він не проникає через плаценту, і його безпека під час вагітності встановлена, таблиця 4.
Незважаючи на те, що в епоху черезшкірного коронарного втручання проведення тромболізису значно зменшилося, тромболітичну терапію слід розглядати у вагітних жінок у відповідних умовах, подібних до невагітних жінок. Однак слід проявляти обережність, враховуючи відсутність контрольованих клінічних випробувань, включно з вагітними жінками, і природу слабкого рівня доказів наявних сукупних даних. Роль використання гепарину для спонтанної дисекції коронарної артерії є суперечливою через потенційний ризик розширення дисекції при використанні антикоагулянтів, які, з іншого боку, можуть бути корисними для розсмоктування тромбу і покращення справжньої прохідності просвіту. Слід уникати тромболітичної терапії при дисекції через повідомлення про шкоду та клінічне погіршення внаслідок розширення інтрамуральної гематоми. Бета-адреноблокатори відіграють важливу роль у фармакологічному арсеналі при лікуванні спонтанної дисекції через їх вплив на зниження навантаження на стінку коронарних артерій [6].
Таблиця 4. Кардіологічні препарати та безпека під час вагітності та лактації.
| Лікарьскі засоби | Чи використовують протягом вагітності? | Примітки при вагітності | Чи використовують протягом періода лактації? |
| Антагоністи альдостерону | Ні | Перетинає плацентарний бар’єр, фемінізація плоду чоловічої статі | Так |
| Інгібітори АПФ/блокатори рецепторів ангіотензіну | Ні | Протипоказані при вагітності у зв’язку з затримкою внутрішньоутробного розвитку, зниження функції нирок плоду, гіпоплазії легень, скелетної мальформації та маловоддя. | Еналаприл чи каптоприл. Не використовуйте БРА. |
| Аспірин | Так | Повну дозу аспірину (325 мг) можна застосовувати до 32 тижнів вагітності, а 81 мг можна застосовувати в будь-який час під час вагітності. Більш високі дози (> 181 мг) асоційовані з високим ризиком кровотечі, вродженими дефектами, передчасним закриттям відкритої артеріальної протоки, із затримкою внутрішньоутробного розвитку, смертю плоду. | Так (81 мг/день) |
| ß-блокатори | Так | Використання метопрололу, лабетололу, карведілолу призводить до затримки внутрішньоутробного розвитку (класс С), неселективні ß-блокатори підвищують активнисть матки. Атенолол перетинає плацентарний бар’єр та призводить до брадікардії плоду, гіпоглікемії, внутрішньоутробна затримка росту плоду, апное, вроджених дефектів. | Так |
| Бівалрудін | Так, якщо потрібно | Інформація обмежена, може визвати патологію матері та плоду | Невідомо |
| Блокатори кальцієвих каналів | Так, якщо потрібно | Тільки ділтіазем не перетинає плацентарний бар’єр. Однако, ділтіазем асоційований з патологію плоду у моделі тварин. Асоційовано з недоношеністю, затримкою внутрішньоутробного розвитку, брадикардією плоду. Корисно при гіпертензії, ішемічних подіях (амлодипін), фібриляція передсердь, коли ß-блокатори протипоказані. Слідкувати за артеріальним тиском, щоб не допустити гіпотензію. | Ніфедипін, інші блокатори кальциєвих каналів потрапляють до до молока |
| Клопідогрель | Так | Клопідогрель можна використовувати протягом вагітності (клас В), потрібно відмінити за 5-7 днів до пологів, якщо планується нейроаксіальна анестезія. Підвищує ризик кровотечі протягом пологів. | Невідомо |
| Фібринолітик | Так, якщо потрібно | Обмежена інформація | Невідомо |
| Інгібіторів глікопротеїну IIb/IIIa | Так, якщо потрібно | Обмежена інформація | Невідомо |
| Гепарин/низькомолекулярні гепарини | Так | Не перетинає плацентарний бар’єр. Добре вивчені без суттєвого ризику. Для гепарину клас С. Для еноксапарину – клас В. | Так |
| Ізосорбід дінітрат | Так | Обмежена інформація | Невідомо |
| Нітрогліцерин | Так | Ризик гіпотензії, зниження маточної та плацентарної гіпоперфузії. | Так |
| Прямі оральні антикоагулянти | Ні | Перетинає плацентарний бар’єр з дуже високим ризиком кровотечі | Невідомо |
| Статини | Ні | Ризик вроджених аномалій | Невідомо |
| Варфарин | Так | Ризик ембріопатії знижується при дозі менш, ніж 5 мг. Якщо потрібні більш високі дози, краще використовувати гепарін перші 12 годин. | Так |
ІАПФ = інгібітор ангіотензинперетворюючого ферменту; БРА = блокатор рецепторів ангіотензину II
*Примітка. Майте на увазі те, що у наведеній вище таблиці використовується попередня система класифікації Food Drug Administration, хоча тепер її переведено на іншу систему класифікації. Нітрати можуть полегшити дискомфорт або усунути/діагностувати спазм коронарних судин, але їх слід застосовувати з обережністю, щоб уникнути гіпотензії матері та плацентарної гіпоперфузії.
Чресшкірне коронарне втручання
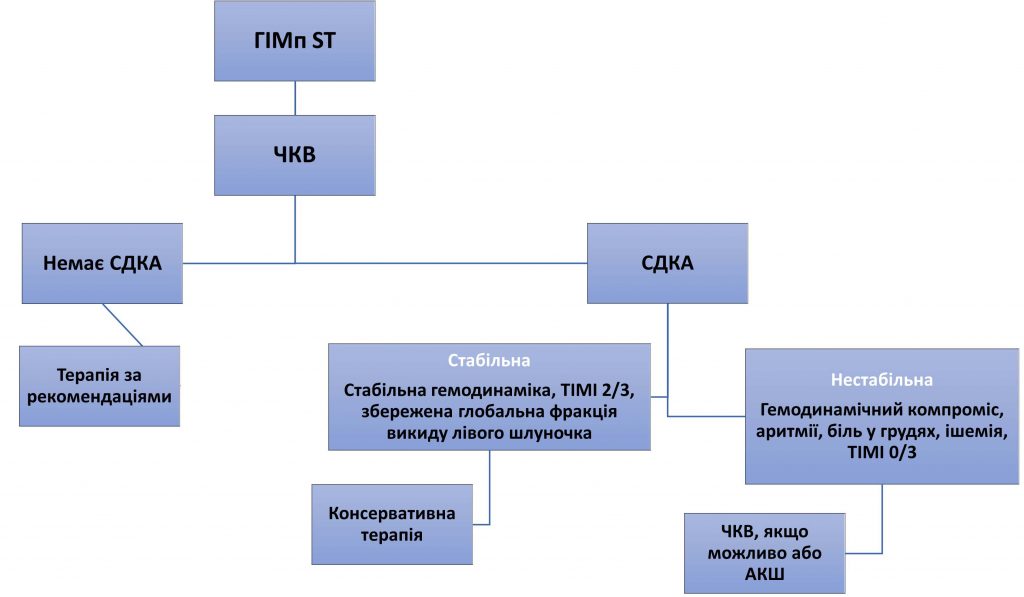
Коронарографія під час вагітності пов’язана з підвищеним ризиком розшарування коронарної артерії, викликаної катетером, особливо в лівій коронарній артерії; цей ятрогенний ризик разом із задокументованою високою частотою спонтанного загоєння розсічених артерій призводить до припущення про консервативне лікування у стабільних пацієнтів із низьким ризиком. Для зниження ризику розшарування рекомендується неселективне введення контрасту в корінь аорти, уникнення глибокої інтубації катетера (особливо при радіальному доступі) і мінімальне використання ін’єкцій під низьким тиском. Запропонований алгоритм лікування дисекції коронарної артерії, асоційованой з вагітністю, наведено на рисунку 6.
(A)
(B)
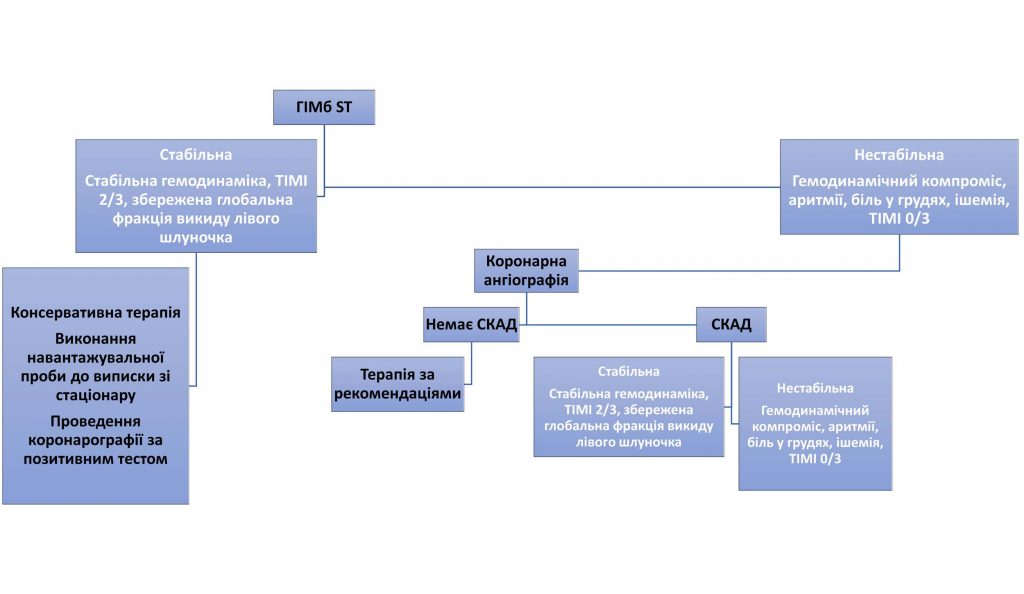
Рисунок 6.Запропоновані алгоритми ведення пацієнтів з інфарктом міокарда, що асоційований з вагітністю: (A) ГІМп ST; (B) ГІМб ST.
ГІМп ST – гострий інфаркт міокарда з підйомом сегмента ST; ЧКВ – чрезшкірне коронарне втручання; СДКА – спонтанна дисекція коронарної артерії, АКШ – аорто-коронарне шунтування; TIMI – Thrombolysis in Myocardial Infarction: TIMI 0 – повна оклюзія коронарної артерії; TIMI 1 – проникнення обструкції за контрастом, але без дистальної перфузії; TIMI 2 – перфузія всієї артерії, але затриманий поток; TIMI 3 – повна перфузія, нормальний поток.
Вплив іонізуючого випромінювання не повинен перешкоджати проведенню первинного ЧКВ у вагітних із стандартними показаннями до реваскуляризації при гострому інфаркті міокарда. Однак дозу радіації необхідно мінімізувати. Слід запровадити радіаційний захист плоду за допомогою свинцевого екранування та заходів щодо зниження радіації. Вплив радіації на плід малоймовірний при дозах нижче 50 мЗв. Враховуючи, що доза опромінення плода, пов’язана з коронарографією, очікується <1 мЗв, ризик радіаційного ураження плоду, ймовірно, незначний у порівнянні з природною частотою вроджених аномалій, таблиця 5.
Таблиця 5. Радіаційна безпека: оцінена доза плода за даними обстеження та порогова доза за гестаційним віком.
| РОЗРАХУНКОВА ДОЗА ОПРОМІНЮВАННЯ ДЛЯ ПЛОДУ (МГР В ЗАЛЕЖНОСТІ ВІД МЕТОДУ ДОСЛІДЖЕННЯ) |
| Рентгенографія органів грудної порожнини (2 проєкції) – 0,0005-0,01 Комп’ютерна томографія в ангіорежимі при ТЕЛА – 0,01-0,66 Коронарна ангіографія – 0,074 Чрезшкірне коронарне втручання – менш ніж 1 Флюорографія від паху до серця – 0,094-0,244 |
| РОЗРАХУНКОВИЙ ПОРІГ ОПРОМІНЮВАННЯ (МГР) В ЗАЛЕЖНОСТІ ВІД ЕФЕКТУ ТА ГЕСТАЦІЙНОГО ПЕРІОДУ (ПОШКОДЖЕННЯ ПЛОДУ) |
| 0-2 тиждень (преімплантація): 50-100 (смерть або ніяких змін) 2-8 тиждень (органогенез): 200-250 (вроджені аномалії чи затримка росту) 8-15 тиждень: 60-310 (тяжкі порушення інтеліктуальної функції, мікроцефалія, дефіцит інтелекту (високий ризик)) 16-25 тиждень: 250-280 (порушення інтеліктуальної функції (низький ризик)) |
ТЕЛА – тромбоемболія легеневої артерії; мгр – мілігрей.
*Кількість енергії, відкладеної на кілограм тканини, вимірюється в мГр, як зазначено вище, тоді як кількість енергії, відкладеної на кілограм тканини, нормалізована щодо біологічної ефективності, вимірюється в мілізівертах. Середньорічний радіаційний фон становить 1,1-2,5 мГр.
Ці оцінки коронарної комп’ютерної томографії в ангіо-режимі, ймовірно, представляють високу межу опромінення плода. Оскільки плід знаходиться за межами первинного променя, розсіювання є основним джерелом випромінювання, і тому очікується, що воно буде низьким. Експозиція плода для зображення грудної клітини збільшується з гестацією через те, що плід знаходиться ближче до основного променя. Дорослі пацієнти вимагають вищої пікової напруги в кіловольтах і струму трубки, що збільшує радіаційне опромінення. Варіанти методів візуалізації, такі як режим сканування та пульсуюче вікно (наприклад, найвужче пульсуюче вікно призводить до найменшої дози), можна оптимізувати для зменшення загального опромінення.
У випадку стабільної гемодинаміки, у хворої низького ризики при гострому коронарному синдромі без підйому сегмента ST слід розглянути неінвазивний підхід. Хоча КТ коронарографія є альтернативним діагностичним підхідом, метод вимагає радіаційного навантаження, потенційно високих доз бета-блокаторів, і може не продемонструвати переваг у випадку диссекції коронарної артерії. Пацієнтам з атеросклеротичним інфарктом міокарда з підйомом сегмента ST рекомендується своєчасна коронарна реперфузія шляхом черезшкірного коронарного втручання [24, 25].
N.B! для інтервенціоналістів
Інтервенціоналісти повинні бути готові до процедурних ускладнень. В одному огляді 5 із 129 (3,8%) вагітних жінок з інфарктом міокарда мали коронарну дисекцію під час ангіографії. Незрозуміло, чи всі це були ятрогенні дисекції, чи деякі з них були загостреннями неідентифікованної дисекції коронарної артерії, чи цей ризик був би подібним у популяційному дослідженні. У пацієнтів також можлива декомпенсація або зупинка серця внаслідок розвитку ішемії під час коронарографії. Якщо коронарографія виконується на життєздатному гестаційному терміні (≥23 тижні), слід розглянути можливість антенатального введення кортикостероїдів і сповіщення чергової акушерської бригади, здатної провести екстрений реанімаційний кесарів розтин у разі декомпенсації з боку матері. Безперервний моніторинг частоти серцевих скорочень плода під час процедури слід проводити лише в тому випадку, якщо можливий негайний кесарів розтин через рефрактерну, невтішну структуру серцевого ритму плода [26].
Вибір стратегії лікування при гострому інфаркті міокарда без підйома сегменту ST
У настановах щодо лікування гострого коронарного синдрому без підйому сегмента ST запропоновано стратегію лікування ішемії без рутинної діагностичної коронарографії для пацієнтів із низьким рівнем ризику (оцінюється за балами ризику, такими як тромболізис при інфаркті міокарда (TIMI) та глобальний реєстр гострих коронарних подій (GRACE); ця рекомендація базується на даних невагітних пацієнток з інфарктом. Останній консенсус Європейського товариства кардіологів пропонує розглянути можливість ведення без інвазивної ангіографії вагітних пацієнток із гострим інфарктом низького ризику з гострим коронарним синдромом без підйому сегмента сегмента ST (рисунок). Однак, показники ризику не включають надмірний ризик, пов’язаний зі станом вагітності/після пологів, і вони не були підтверджені в популяції.
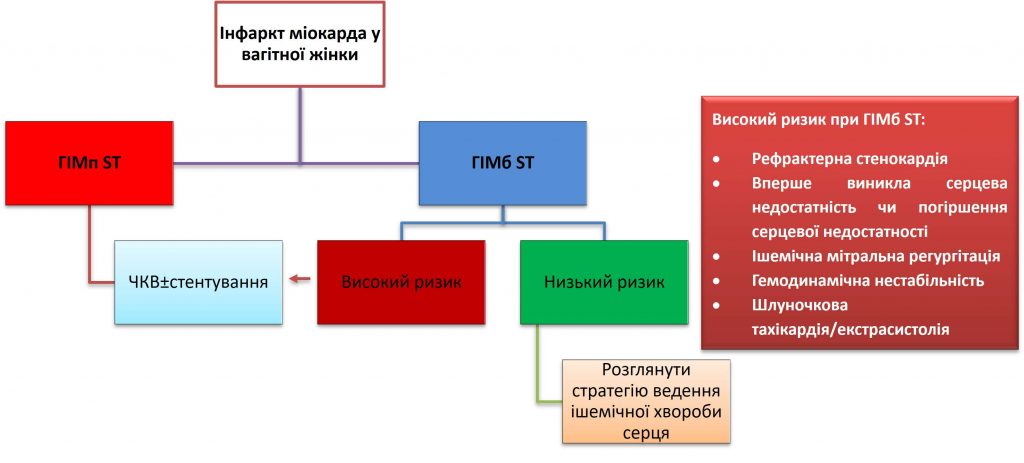
Коронарна комп’ютерна томографія – це неінвазивний альтернативний метод діагностики, який слід розглядати у пацієнток з низьким ризиком, хоча обмеження включають можливість отримання непереконливих результатів через обмежену роздільну здатність або артефакт руху. Виявлення причини інфаркту визначає майбутну стратегію ведення пацієнтки, навіть якщо реваскуляризація не виконується. Таким чином, слід розглянути можливість проведення інвазивної діагностичної коронарної ангіографії, якщо очікувані ризики не переважають передбачувані переваги у пацієнток з низьким ризиком, наприклад у пацієнток із зниклими симптомами та негативними або помірно підвищеними серцевими біомаркерами, рисунок 7 [6,27].
Рисунок 7. Стратегія лікування інфаркту міокарда, пов’язаного з вагітністю.
ГІМп ST – гострий інфаркт міокарда з підйомом сегмента ST; ГІМб ST – гострий інфаркт міокарда без підйома сегмента ST; ЧКВ – чрезшкірне коронарне втручання
Вибір стента та антитромбоцитарна терапія
У більшості випадків при гострому інфаркті міокарда з підйомом сегмента ST під час вагітності застосовуються непокриті металеві стенти. Однак стенти з лікарським покриттям (DES) нового покоління є рекомендованими відповідно до рекомендацій 2017 року при гострому інфаркті міокарда з підйомом сегмента ST. Оскільки жодних ускладнень при прийомі аспірину та клопідогрелю у стентованих вагітних не було, застосування більш потужного інгібітора P2Y12 слід розглядати з обережністю через високий ризик кровотечі. Тривалість подвійної антиагрегантної терапії при використанні стента з лікарським покриттям другого та третього покоління може бути скорочена, особливо за відсутності значущого тромботичного навантаження. Повідомлялося про використання біорозсмоктуваних стентів при спонтанній дисекції коронарної артерії; однак наразі немає впевнених доказів, щоб рекомендувати їх під час вагітності.
Аортокоронарне шунтування може розглядатися у пацієнток із показаннями до коронарної реваскуляризації, які є поганими кандидатами для черезшкірного коронарного втручання на основі рекомендацій для невагітних дорослих. У пацієнтів із спонтанною дисекцією коронарної артерії слід розглянути можливість аортокоронарного шунтування, якщо вважається, що черезшкірне коронарне втручання створює підвищений ризик, наприклад, спонтанна дисекція лівої магістральної або двосудинної коронарної артерії, або як допоміжну терапію у випадках невдачі ЧКВ. Артеріальні трансплантати оптимізують довговічність реваскуляризації та часто є кращими для пацієнтів з атеросклеротичним інфарктом. У пацієнтів зі спонтанною дисекцією коронарної артерії венозні або артеріальні трансплантати можуть оклюзуватися або стати атретичними після загоєння нативної судини та відновлення конкурентного кровотоку. Таким чином, прийняття рішення щодо трансплантатів серед пацієнтів зі спонтанною дисекцією коронарної артерії вимагає оцінки в кожному конкретному випадку.
Кардіогенний шок, застійна серцева недостатність і зупинка серця
У звіті про 150 жінок з інфарктом міокарда, пов’язаним з вагітністю, у 38% розвинувся шок або застійна серцева недостатність. У цих пацієнтів високого ризику з нестабільністю гемодинаміки під час вагітності застосовували механічну підтримку кровообігу за допомогою внутрішньоаортальних балонних насосів, черезшкірних вентрикулярних допоміжних пристроїв і екстракорпоральних мембранних оксигенаторів, які вважаються заходами для порятунку життя. У разі зупинки серця невідкладна високоякісна серцево-легенева реанімація принесе найбільшу користь для матері та плоду. Пацієнти повинні лежати на спині на твердій поверхні, а серцево-легенева реанімація виконується згідно зі стандартним протоколом. Немає необхідності замінювати ліки або змінювати дозу. Рекомендації, що стосуються вагітності, включають безперервне ручне зміщення матки вліво, щоб зняти навантаження від аортокавального стиснення під час серцево-легеневої реанімації, внутрішньовенний доступ у вену над діафрагмою, щоб гарантувати, що вагітна матка не перешкоджає терапії, і повну підготовку до проведення негайного реанімаційного кесаревого розтину в разі повернення спонтанний кровообіг не досягається через 4 хвилини реанімації. Серцево-легеневу реанімацію матері необхідно продовжувати з мінімальними перервами під час підготовки та проведення кесаревого розтину. Розродження за допомогою кесаревого розтину слід проводити на місці зупинки, якщо це можливо, щоб найкраще оптимізувати стан матері [6,27].
Коронарографія та лікування спонтанної дисекції коронарної артерії
Лікування спонтанної дисекції коронарної артерії, що асоційована з вагітністю подібне до спонтанної дисекції коронарної артерії у невагітних пацієнток; однак результати під час вагітності гірші, що вимагає особливої обережності при оцінці та веденні таких пацієнток. Консервативній терапії надають перевагу у більшості стабільних пацієнтів зі спонтанною дисекцією коронарної артерії на фоні вагітності, оскільки чрезшкірне коронарне втручання часто асоціюється з розповсюдженням розшарувань. У гемодинамічно нестабільних жінок можна розглянути можливість механічної підтримки за допомогою внутрішньоаортального балонного насоса, таблиця 6.
Таблиця 6. Прояви та лікування спонтанної дисекції коронарної артерії під час вагітності
| Презентація | Спонтанна дисекція коронарної артерії найчастіше виникає після пологівЛіва передня низхідна коронарна артерія є найбільш часто ураженою судиноюСпонтанна дисекція коронарної артерії частіше проявляється багатосудинною дисекцією та порушенням гемодинаміки порівняно з невагітними хворими зі спонтанною дисекцією |
| Оцінка | Ретельна ангіографія, щоб уникнути поширення розшаруванняВнутрішньосудинна візуалізація може підтвердити діагноз, хоча слід враховувати ризик поширення дисекції, особливо в дрібних звивистих судинах |
| Консервативне лікування | • Консервативній терапії надають перевагу у більшості стабільних пацієнтів із спонтанною дисекцією коронарної артерії, оскільки ЧКВ часто асоціюється з поширенням дисекції • Довгострокова терапія включає аспірин і бета-блокатори з неясною роллю подвійної антитромбоцитарної терапії • Внутрішньовенне введення гепарину слід припинити після виявлення спонтанної дисекції коронарної артерії • Інгібітори глікопротеїну IIb/Illa та тромболітики протипоказані через можливе розширення інтрамуральної гематоми |
| Інвазивне втручання | Показання до ЧКВ або АКШ включають триваючу ішемію та інфаркт, гемодинамічну нестабільність і розшарування лівої коронарної артеріїАКШ, як правило, показано для лівої головної дисекції або невдалого ЧКВ у нестабільних пацієнтівМеханічну підтримку за допомогою внутрішньоаортального балонного насоса можна розглядати у гемодинамічно нестабільних пацієнтів |
Пологи
Припускаючи гемодинамічну стабільність, терміни пологів можуть залежати від гестаційного віку на момент початкової події, поточного стану серця матері та очікуваного ступеня тимчасового відновлення, наявності ключового персоналу та ресурсів, а також майбутніх потреб у антикоагулянтах. З практичної точки зору, пологи слід відкласти (якщо можливо) щонайменше на 2 тижні після гострої коронарної події. Розродження здійснюється як через природні родові шляхи, так і оперативним шляхом. Розродження через природні родові шляхи дозволяє уникнути потенційних ризиків, пов’язаних з анестезією, що безпечно за умови стабільного стану гемодинаміки хворої. Оперативне розродження здійснюється як під загальною, так і під регіонарною (найчастіше) анестезією з моніторуванням ЕКГ та АТ, пульсоксиметрією. За відсутності специфічних передпологових ускладнень у матері або плода пологи проводяться за стандартними акушерськими показаннями: або обирається термін вагітності від 39 до 40 тижнів, або очікуються спонтанні пологи. Плановий кесарів розтин не приносить ні акушерської, ні серцево-судинної користі, і перевага віддається вагінальним пологам. Однак, якщо жінка починає пологи під час терапії антикоагулянтами варфарином, кесарів розтин є кращим через ризик церебрального крововиливу плода під час вагінальних пологів.
Слід уникати застосування певних акушерських препаратів. Що стосується інтранатальної аналгезії, можна використовувати нейроаксіальний анестетик, якщо пацієнтка приймає лише аспірин, але не приймає подвійну антиагрегантну терапію. Інгібітор P2Y12 слід припинити за 7 днів до пологів, якщо це безпечно. Кардіологічний протокол під час пологів може включати
- раннє введення нейроаксіальної анестезії;
- встановлення артеріального катетера для прямого моніторингу артеріального тиску;
- ретельний контроль рідини;
- безперервний телеметричний моніторинг (у відповідних випадках);
- відстрочені маневри Вальсальви на другому етапі пологів для оптимізації серцевого викиду та безперервного серцевого венозного повернення з оперативними вагінальними пологами (щипці, вакуум, інші допоміжні пристрої) виключно за стандартними показаннями; і
- уникнення надмірної крововтрати.
Несприятливі наслідки вагітності, такі як передчасні пологи, гестаційна гіпертензія та прееклампсія, гестаційний цукровий діабет та малий гестаційний вік, є групою взаємопов’язаних розладів, які мають загальні шляхи розвитку та, як вважають, спричинені плацентарною дисфункцією та окисним стресом. Ці несприятливі наслідки вагітності пов’язані з підвищеним ризиком майбутніх серцево-судинних захворювань (гіпертонія, ішемічна хвороба серця, інсульт) і включені в рекомендації 2018 року щодо контролю рівня холестерину в крові як станів, що підвищують ризик серцево-судинних захворювань. Пацієнтки вимагають подальшого спостереження в четвертому триместрі, у цей час слід провести агресивну модифікацію факторів ризику та обговорити майбутні ризики з пацієнткою.
Жінки з попередньо встановленою ішемічною хворобою серця або гострим коронарним синдромом/інфарктом міокарда в анамнезі, мають ризик серйозних
несприятливих серцевих подій під час вагітності, ризик яких є найвищим при атеросклеротичній коронарній хворобі з рівнем материнської смертності між 0–23%. Несприятливі акушерські результати зустрічаються приблизно в 16%, при цьому 30% вагітностей ускладнюються несприятливими подіями у плоду та в подальшому неонатальному періоді. Немає якісних даних, які б визначали, наскільки повинна бути відтермінована вагітність після гострого інфаркту міокарда, однак, рекомендації 12 місяців здаються обґрунтованими. Не існує остаточних доказів того, що попередня диссекція коронарної артерії підвищує ризик рецидиву. Проте рекомендується уникати подальшої вагітності і, якщо пацієнтка вирішує продовжити планування вагітності, рекомендується ретельний моніторинг, таблиця 7.
Таблиця 7. Розгляд акушерської терапії у жінок з інфарктом міокарда, пов’язаним з вагітністю
| Препарати | Чи використовуються при вагітності | Показання | Застереження |
| Внутришньоутробні кортікостероїди (бетаметазон, дексаметазон) | Так | Слід використовувати, якщо пологи очікуютьмя протягом найближчих 7 днів; курс містить бетаметазон (12 мг кожні 24 годині по 2 дози) та можно повторити одноразово до 34 тижня, якщо немає пердчасних пологів чи є високий ризик | Хоча будь-який препарат може проявляти мінералокортикоїдну активність у невеликому ступені, затримка рідини та набряк легенів були описані лише за інших обставин (токолітична терапія, багатоплідна вагітність, внутрішньоплідна інфекція). Минуча гіперглікемія у хворих з діабетом. |
| Карбопрост трометамин | З обережністю | Утеротонічна медикаментозна терапія для лікування післяпологової кровотечі | Може призвести до вторинної гіпертензії |
| Сульфат мгнезії | Так | Вводиться внутрішньовенно задля нейропротекції плоду до 32 тижня вагітності, для профілактики судом хворим з прееклампсією та еклампсією, та нечасто задля токолітичного ефекту. | Може призвести до гіпотонії та брадікардії. |
| Метилергоновін малеат | Ні | Утеротонічна медикаментозна терапія для лікування післяпологової кровотечі | Може призвести до коронарного спазу, тому слід уникати |
| Оксітоцин | З обережністю | Звичайно призначається для збільшення скорочування матки, частіше при пологах або у ранньому післяпологовому періоді | Використання асоційоване з гіпотонією та шлуночковими аритміями |
| Тербуталін | Ні | Лікарський засіб з ß-міметичними властивостями, яке використовують під час пологів при маткової тахісистолії (надмірна частота скорочень) | Часті побічні явища – це тахікардія та аритмії |
| Транексаміновая кислота | Ні | Антифібрінолітичний агент, що використовують для підвищення гемостазу при лікуванні післяпологової кровотечі | При активному тромбозі протипоказано |
Для пацієнтів, які не є кандидатами на регіонарну анестезію або відмовляються від неї, внутрішньовенні опіоїдні анальгетики (фентаніл, меперидин, морфін) є варіантом другої лінії терапії, визнаючи, що жоден не надає подібних гемодинамічних переваг, як нейроаксіальна анестезія.
Наразі існує мінімальна кількість даних щодо безпеки інгаляційного закису азоту, який має неоднакову ефективність для зменшення болю. Закис азоту пов’язаний з пригніченням скоротливої здатністі міокарда та транзиторною легеневою гіпертензією, хоча високий ризик післяопераційних серцевих подій не спостерігався у невагітних хірургічних груп. В очікуванні значного фізіологічного внутрішньосудинно-екстраваскулярного перерозподілу рідини у пацієнтів із інфарктом зазвичай спостерігають у відділенні інтенсивної терапії протягом перших 24–48 годин після пологів.
Невідкладна терапія післяпологового інфаркту міокарда
Невідкладне лікування інфаркту у післяпологовому періоді є більш простим, ніж у допологовий період, оскільки ризики для плода більше не є актуальними. Ризик кровотечі у матері може зберігатися відразу після пологів, але очікується, що з часом він зменшиться. Міркування щодо коронарної реваскуляризації при післяпологовому інфаркті такі ж, як і у невагітних жінок, таблиця 8.
| Оцінка перед зачяттям | Передпологовий менеджмент | Післяпологове довгострокове лікування | |
| Ішемічна хвороба серця | ЧКВ/ІМ в анамнезіОцінка медикаментозної терапіїї ІХСОцінка наявних симптомів | Оцінка можливого ГКСРоглядати можливе проведення ЧКВЗастосування антитромбоцитарної терапії | КонтрацепціяКонсультативна допомога щодо планування майбутньої вагітностіТривала модифікація ризику серцево-судинних захворювань |
| Кардіоміопатія | Кардіоміопатія в анамнезіОцінити лікування серцевої недостатностіФункціональний клас та міокардіальний резерв | Лікування гострої серцевої недостатностіКоригування медикаментозного лікування після пологівАнтикоагулянтна терапія у жінок с післяродовою кардіоміопатією | |
| Аритмія | Анамнез імплантованого пристроюАритмії в анамнезіОцінка наявних антиаритмічних засобів, антикоагулянтів | Невідкладне лікування аритмійРозгляд абляції при гострих рефрактерних аритміях | |
| Гіпертонічні розлади вагітності | Хронічна гіпертензія в анамнезіКоригування антигіпертензивних препаратівПопередження прееклампсії за допомогою малих доз ацетилсаліцилової кислоти | Лікування гострої та тяжкої гіпертензіїКоригування медикаментозної терапії після пологівКонтроль артеріального тиску після пологів |
Таблиця 8. Лікування складних набутих і спадкових серцево-судинних захворювань під час вагітності та міркування щодо спеціальної серцево-судинної допомоги. Багатопрофільна експертиза: гіпертензія, інтервенція, електрофізіологія та серцева недостатність
Грудне вигодовування після коронарної події
Загальні рекомендації щодо лактації слід адаптувати до конкретної пацієнтки, хоча більшість ліків проникає в грудне молоко. Якщо плануються подальші рентгенографічні дослідження з використанням йодовмісного контрасту, лактацію не потрібно переривати, оскільки <1% виділяється в грудне молоко. Інші стратегії лікування після інфаркту міокарда на тлі вагітності описані в таблиці 9.
Таблиця 9. Амбулаторне лікування після інфаркту міокарда, пов’язаного з вагітністю.
| Рекомендації після коронарнох події | Раціональність |
| Скринінг та лікування тривоги, депресії та післяпологового стресового розладу | Післяродова депресія виникає у 13% випадків та пов’язана з захворюванністю та смертністю |
| Кардіологічна реабілітація | Кардіалогічна реабілітація знижає прояви тривоги та депресії, підвищує якість життя, виживаність та зниження ризику півторного інфаркту міокарда. |
| Модифікація факторів риизку: АТ менш 130/80 мм рт ст, відмовитися від тютюнопаління, контроль рівню ліпідів крові, здорове харчування та фізичні вправи | Ця стратегія підвищує загальне здоров’я та знижає кардіоваскулярний ризик. |
| ß-блокатори та інгібітори АПФ повинні бути призначені, особливо тим хворим, що мають систолічну дисфункцію | Зниження навантаження та прискорення відновлення після інфаркту |
| Додаткові зауваження | |
| Атеросклероз: подвійна антитромбоцитарна терапія незалежно від стентування протягом 12 місяців та аспірин бесстроково. Високо інтенсивні дози статинів, якщо не кормить груддю. | |
| Коронарний емболізм: використування оральних антикаогулянтів. | |
| Спонтанна дисекція коронарної артерії: подвійна антитромбоцитарна терапія протягом 12 місяців, якщо проведене стентування. Статини, якщо не кормить груддю. Оцінити наявність хвороб сполучної тканини (фібромаскулярна дисплазія, артеріопатія). | |
Майбутня вагітність
Доцільність вагітності залежить від основної причини та ступеня дисфункції лівого шлуночка. Дві невеликі серії досліджень з 1990-х років описують частоту ускладнень у матері від 71% до 100% із загальними наслідками затримки розвитку плода. У більш сучасній серії було виявлено 10% частоту рецидивів значних серцевих ускладнень зі смертністю до 23% і підвищену частоту післяпологових кровотеч і загибелі плода/новонародженого. Жодна з основних стратегій стратифікації ризику серцево-судинних захворювань (оцінка ризику серцевих захворювань під час вагітності [ZAHARA], модифікована Всесвітнею організацією охорони здоров’я) не індексує інфаркт міокарда на тлі вагітності конкретно, хоча тяжка системна шлуночкова дисфункція (фракція викиду лівого шлуночка <30%) зазначена як протипоказання до вагітності в модифікованій класифікації Всесвітньої організації охорони здоров’я. Консенсус Європейського товариства кардіологів показує, що вагітність може бути розглянута без клінічних ознак стійкої дисфункції лівого шлуночка або ішемії, з рекомендацією відкласти зачаття на 12 місяців після коронарної події. Якщо попередній інфаркт був спричинений дисекцією, консенсус полягав у тому, щоб рекомендувати уникати майбутньої вагітності, усвідомлюючи, що може відігравати роль індивідуальне консультування.
Висновки
Вагітні жінки з гострим інфарктом представляють унікальну популяцію пацієнтів, для якої необхідне ретельне вивчення причин, обдумане та доцільне прийняття рішення про лікування та уважний амбулаторний догляд. Ці заходи разом із вхідними даними мультидисциплінарної групи кардіологів вагітних є доречними для персоналізваного догляду за вказівками з опублікованих досліджень, консенсусних документів і попереднього досвіду.
Зареєструйтеся на нашому сайті прямо зараз, щоб мати доступ до більшої кількості навчальних матеріалів!
Підписатися на наші сторінки:
Джерела:
- Merlo AC, Rosa GM, Porto I. Pregnancy-related acute myocardial infarction: a review of the recent literature. Clin Res Cardiol. 2022 Jul;111(7):723-731. doi: 10.1007/s00392-021-01937-5. Epub 2021 Sep 12. PMID: 34510263; PMCID: PMC9242969
- Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, Blomström-Lundqvist C, Cífková R, De Bonis M, Iung B, Johnson MR, Kintscher U, Kranke P, Lang IM, Morais J, Pieper PG, Presbitero P, Price S, Rosano GMC, Seeland U, Simoncini T, Swan L, Warnes CA; ESC Scientific Document Group. 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy. Eur Heart J. 2018 Sep 7;39(34):3165-3241. doi: 10.1093/eurheartj/ehy340. PMID: 30165544.
- Ki Park, C. Noel Bairey Merz, Natalie A. Bello, et al., Management of Women With Acquired Cardiovascular Disease From Pre-Conception Through Pregnancy and Postpartum: JACC Focus Seminar 3/5, Journal of the American College of Cardiology, Volume 77, Issue 14, 2021, Pages 1799-1812, https://doi.org/10.1016/j.jacc.2021.01.057;
- J.Roos-Hesselink, L.Baris, M. Johnson, et al. Pregnancy outcomes in women with cardiovascular disease: evolving trends over 10 years in the ESC Registry of Pregnancy and Cardiac Disease (ROPAC) Eur Heart J.40(2019), pp.3848-3855
- Mehta L, Warnes CA, Bradley E, et al. American Heart Association Council on Clinical Cardiology; Council on Arteriosclerosis, Thrombosis and Vascular Biology; Council on Cardiovascular and Stroke Nursing; and Stroke Council. Cardiovascular considerations in caring for pregnant patients: A scientific statement from the American Heart Association. Circulation. 2020;141:e884–e903. https://doi.org/10.1161/CIR.0000000000000772
- Tweet MS, Lewey J, Smilowitz NR, Rose CH, Best PJM. Pregnancy-Associated Myocardial Infarction: Prevalence, Causes, and Interventional Management. Circ Cardiovasc Interv. 2020 Aug 1:CIRCINTERVENTIONS120008687. doi: 10.1161/CIRCINTERVENTIONS.120.008687. Epub ahead of print. PMID: 32862672; PMCID: PMC7854968;
- Gibson P, Narous M, Firoz T, Chou D, Barreix M, Say L and James M. Incidence of myocardial infarction in pregnancy: a systematic review and meta-analysis of population-based studies. Eur Heart J Qual Care Clin Outcomes. 2017;3:198–207.
- Quesada O, Scantlebury DC, Briller JE, Michos ED, Aggarwal NR. Markers of Cardiovascular Risk Associated with Pregnancy. Curr Cardiol Rep. 2023 Feb;25(2):77-87. doi: 10.1007/s11886-022-01830-1. Epub 2023 Feb 6. PMID: 36745273; PMCID: PMC10278153
- Garcia M, Mulvagh SL, Merz CN, Buring JE, Manson JE. Cardiovascular Disease in Women: Clinical Perspectives. Circ Res. 2016 Apr 15;118(8):1273-93. doi: 10.1161/CIRCRESAHA.116.307547. PMID: 27081110; PMCID: PMC4834856.
- Silversides CK, Grewal J, Mason J, Sermer M, Kiess M, Rychel V, Wald RM, Colman JM, Siu SC. Pregnancy Outcomes in Women With Heart Disease: The CARPREG II Study. J Am Coll Cardiol. 2018 May 29;71(21):2419-2430. doi: 10.1016/j.jacc.2018.02.076. PMID: 29793631.
- Crousillat, D., Park, K., Wood, M.J. (2023). Acute Coronary Syndrome in Pregnancy. In: Sharma, G., Scott, N.S., Davis, M.B., Economy, K.E. (eds) Contemporary Topics in Cardio-Obstetrics. Contemporary Cardiology. Humana, Cham. https://doi.org/10.1007/978-3-031-34103-8_15
- https://obgynkey.com/acute-coronary-syndromes-in-pregnancy/
- Marysia S. Tweet. Circulation: Cardiovascular Interventions. Pregnancy-Associated Myocardial Infarction, Volume: 13, Issue: 11, DOI: (10.1161/CIRCINTERVENTIONS.120.008687)
- Elkayam U, Jalnapurkar S, Barakkat MN, Khatri N, Kealey AJ, Mehra A, Roth A. Pregnancy-associated acute myocardial infarction: a review of contemporary experience in 150 cases between 2006 and 2011.Circulation. 2014; 129:1695–1702. doi: 10.1161/CIRCULATIONAHA.113.002054
- Gibson P, Narous M, Firoz T, Chou D, Barreix M, Say L, James M; WHO Maternal Morbidity Working Group. Incidence of myocardial infarction in pregnancy: a systematic review and meta-analysis of population-based studies.Eur Heart J Qual Care Clin Outcomes. 2017; 3:198–207. doi: 10.1093/ehjqcco/qcw060
- Tweet MS, Hayes SN, Codsi E, Gulati R, Rose CH, Best PJM. Spontaneous coronary artery dissection associated with pregnancy.J Am Coll Cardiol. 2017; 70:426–435. doi: 10.1016/j.jacc.2017.05.055
- Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, Blomström-Lundqvist C, Cífková R, De Bonis M, Iung B, Johnson MR, Kintscher U, Kranke P, et al; ESC Scientific Document Group. 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy.Eur Heart J. 2018; 39:3165–3241. doi: 10.1093/eurheartj/ehy340
- Lau ES, Sarma A. The Role of Cardiac Biomarkers in Pregnancy.Curr Treat Options Cardiovasc Med. 2017; 19:49. doi: 10.1007/s11936-017-0553-3
- Tamis-Holland JE, Jneid H, Reynolds HR, Agewall S, Brilakis ES, Brown TM, Lerman A, Cushman M, Kumbhani DJ, Arslanian-Engoren C, et al; American Heart Association Interventional Cardiovascular Care Committee of the Council on Clinical Cardiology; Council on Cardiovascular and Stroke Nursing; Council on Epidemiology and Prevention; and Council on Quality of Care and Outcomes Research. Contemporary diagnosis and management of patients with myocardial infarction in the absence of obstructive coronary artery disease: a scientific statement from the American Heart Association.Circulation. 2019; 139:e891–e908. doi: 10.1161/CIR.0000000000000670
- Adlam D, Alfonso F, Maas A, Vrints C; Writing Committee. European society of cardiology, acute cardiovascular care association, SCAD study group: a position paper on spontaneous coronary artery dissection.Eur Heart J. 2018; 39:3353–3368. doi: 10.1093/eurheartj/ehy080
- Oindi FM, Sequeira E, Sequeira HR, Mutiso SK. Takotsubo cardiomyopathy in pregnancy: a case report and literature review.BMC Pregnancy Childbirth. 2019; 19:89. doi: 10.1186/s12884-019-2233-7
- Hausvater A, Smilowitz NR, Saw J, Sherrid M, Ali T, Espinosa D, Mersha R, DeFonte M, Reynolds HR. Spontaneous coronary artery dissection in patients with a provisional diagnosis of takotsubo syndrome.J Am Heart Assoc. 2019; 8:e013581. doi: 10.1161/JAHA.119.013581
- Bird ST, Gelperin K, Sahin L, Bleich KB, Fazio-Eynullayeva E, Woods C, Radden E, Greene P, McCloskey C, Johnson T, et al. First-trimester exposure to gadolinium-based contrast agents: a utilization study of 4.6 Million U.S. pregnancies.Radiology. 2019; 293:193–200. doi: 10.1148/radiol.2019190563
- Mervak BM, Altun E, McGinty KA, Hyslop WB, Semelka RC, Burke LM. MRI in pregnancy: indications and practical considerations.J Magn Reson Imaging. 2019; 49:621–631. doi: 10.1002/jmri.26317
- Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, Byrne RA, Collet JP, Falk V, Head SJ, et al; ESC Scientific Document Group. 2018 ESC/EACTS Guidelines on myocardial revascularization.Eur Heart J. 2019; 40:87–165. doi: 10.1093/eurheartj/ehy394
- Pacheco LD, Saade GR, Hankins GDV. Extracorporeal membrane oxygenation (ECMO) during pregnancy and postpartum.Semin Perinatol. 2018; 42:21–25. doi: 10.1053/j.semperi.2017.11.005
- Centers for Disease Control and Prevention. Pregnancy Mortality Surveillance System.https://www.cdc.gov/reproductivehealth/maternal-mortality/pregnancy-mortality-surveillance-system.htm. Updated February 4, 2020. Accessed April 23, 2020.
Запальна дилятаційна кардіоміопатія
Автор матеріалу: Кардіоміопатія – це патологія міокарду, що характеризується структурно-функціональними порушеннями, які не пов’язані з…
OMI-NOMI vs STEMI-NSTEMI. Час для зміни парадигми?
Дві парадигми однієї нозології OMI-NOMI vs STEMI-NSTEMI Останніми роками накопичилися дані за результатами проведених клінічних…
Аритмогенна кардіоміопатія
Аритмогенна кардіоміопатія (АКМП) – це спадкове захворювання, що характеризується фіброзно-жировим заміщенням міокарда правого шлуночка (ПШ)…
Інфекційний ендокардит. Діагностичні критерії інфекційного ендокардиту
Інфекційний ендокардит (ІЕ) визначається як інфекція ендокардіального шару серця, в першу чергу 1 або декількох…
Синдром ранньої реполяризації шлуночків
Рання реполяризація шлуночків впродовж тривалого часу вважалася доброякісним феноменом, який зустрічається приблизно у 10% населення…
Синдроми J-хвилі. Синдром Бругада
Точка J ‒ це точка переходу комплексу QRS у сегмент ST. На електрофізіологічному рівні вона…