Консультування пацієнта з підозрою на токсичний гепатит – рекомендації ОСКІ
Автори: Самойлова Ганна, Лопіна Наталія
Початок консультації
- Вимийте руки та при необхідності надіньте ЗІЗ (засоби індивідуального захисту)
- Представтеся пацієнту, вказуючи своє ім’я та посаду
- Підтвердіть прізвище, ім’я, по батькові та дату народження пацієнта
- Поясніть пацієнту мету консультації та процедури, що включатиме обстеження, використовуючи зрозумілу для пацієнта мову.
- Отримайте згоду на консультування та надання медичної допомоги
З’ясування основних скарг
- Використовуйте відкриті запитання, щоб вивчити скарги пацієнта
- Деталізація основних скарг
- Проаналізуйте роздуми, побоювання та очікування пацієнта
- Резюмуйте скарги пацієнта
Комплексна оцінка
- Проведіть оцінку інших симптомів для отримання комплексної картини
Збір анамнестичних даних
Збір анамнезу захворювання
- З’ясуйте коли вперше з’явилися симптоми хвороби, які були перші ознаки
- З’ясуйте, які симптоми пацієнт має зараз, як вони змінюються протягом часу
- З’ясуйте, чи скаржиться пацієнт на біль у животі
- З’ясуйте, де саме присутній цей біль (в якій ділянці живота)
- З’ясуйте, чи є у пацієнта порушення апетиту
- З’ясуйте, чи є у пацієнта нудота та\або блювання
- З’ясуйте, чи турбує пацієнта загальна слабкість та підвищена стомлюваність
- З’ясуйте, чи змінювався у пацієнта колір шкіри та слизових оболонок
- З’ясуйте, чи змінювався у пацієнта колір сечі та\або калу
- З’ясуйте, чи турбує пацієнта печія
- З’ясуйте, чи турбує пацієнта свербіж шкіри
- З’ясуйте, чи турбує пацієнта біль у суглобах
- З’ясуйте, чи турбує пацієнта наявність гематом на тілі
- З’ясуйте, чи збільшувався у об’ємі живіт пацієнта
- Спитайте чи звертався пацієнт за медичною допомогою, якщо так, то до кого та чим завершилось його звернення, якщо ні, то уточніть чому не звертався; чи приймав пацієнт самостійно або за призначенням лікаря медичні препарати, якщо так, то, чи змінювався характер скарг на тлі лікування
- У випадку госпіталізації з приводу даних скарг, ознайомтесь з випискою з історії хвороби пацієнта, зверніть увагу на встановлений клінічний діагноз, результати проведених лабораторних та/або інструментальних обстежень, проведене лікування та рекомендації після виписки, а також чи дотримувався пацієнт призначеної схеми лікування
- У випадку проведення пацієнту раніше лабораторних та/або інструментальних обстежень з приводу поточних скарг, проаналізуйте їх результати та вкажіть на важливі знахідки
- З’ясуйте, що спонукало пацієнта звернутися за консультацією цього разу
- Виключіть інші причини наявних скарг, ставлячи пацієнту уточнюючі питання.
Збір анамнезу життя
- З’ясуйте наявність у хворого хронічних захворювань, зокрема неврологічних, ендокринних захворювань, захворювань шлунково-кишкового тракту чи нирок тощо
- Уточніть перенесені пацієнтом інфекційні захворювання
- Уточніть, чи проводились пацієнту раніше оперативні втручання
- З’ясуйте, чи були вагітності, роди або кесарів розтин, чи є зараз грудне вигодовування
- З’ясуйте час настання менопаузи та прийом замісної гормональної терапії
- З’ясуйте, чи приймає пацієнт постійно лікарські препарати та які саме, вкажіть дози препаратів
- Уточніть, чи переносив пацієнт раніше травми, з’ясуйте, як протікав відновлювальний період
- З’ясуйте чи є у пацієнта непереносимість лікарських препаратів або продуктів харчування та уточніть, як саме вона проявляється
- Уточніть, чи є у пацієнта шкідливі звички-вживання алкоголю, наркотичних речовин, паління
- З’ясуйте рівень фізичної активності пацієнта
- З’ясуйте сімейний стан пацієнта, побутові умови проживання; уточніть, чи не було серед кровних родичів випадків міастенії та/або інших захворювань, що проявлялися м’язовою слабкістю
- З’ясуйте, чи працює пацієнт, його професію, умови роботи, наявність шкідливих факторів
Фізикальне обстеження
Оцінка загального стану пацієнта
- Проведення загального огляду
- Оцінка конституції
- Оцінка ступеня вгодованості
- Окружність талії
- Шкіра
- Слизові оболонки
- Щитоподібна залоза
- Оцінка периферійних лімфовузлів
- Оцінка органів дихання
- Оцінка серцево-судинної системи
- Оцінка органів черевної порожнини
- Оцінка органів сечостатевої системи
Оцінка пацієнта за шкалами
- Оцінка термінальної стадії захворювання печінки MELD (за потреби) https://clincasequest.academy/meld-score/ (за потреби)
- Визначення R-значення для оцінки типу ураження печінки. https://clincasequest.academy/r-value/ (за потреби)
- Шкала Чайлд-П’ю для оцінки смертності від цирозу печінки https://clincasequest.academy/child-pugh-score/ (за потреби)
- Шкала RUCAM для оцінки ймовірності медикаментозного ураження печінки DILI/HILI (за потреби)
Призначення лабораторного обстеження
- Загальний аналіз крові (обов’язково)
- Аналіз крові на електроліти (калій, кальцій, натрій) (обов’язково)
- Аналіз крові білкових фракцій крові (обов’язково)
- Аналіз крові на рівень глюкози натщесерце (обов’язково)
- Аналіз крові на печінкові проби (обов’язково)
- Аналіз крові на ліпідний спектр (обов’язково)
- Аналіз крові на ниркові проби (обов’язково)
- Аналіз крові на рівень заліза (за потреби)
- Аналіз крові на рівень вітаміну В12 (за потреби)
- Імунологічне дослідження крові (обов’язково)
- Імуноферентне дослідження та ПЛР маркери вірусних гепатитів (вірусні гепатити А,В,С,Е, викликані вірусом Епштейна-Барр, цитомегаловірусом, вірусом гересу) (обов’язково)
- Тест Фібромакс ™ (FibroMax, FM) (обов’язково)
- Тест на антинуклеарні антитіла (за потреби)
- Аналіз крові на рівень міді (за потреби)
- Аналіз крові на церулоплазмін (за потреби)
- Аналіз сечі на рівень міді (за потреби)
- Коагулограмма (обов’язково)
- Аналіз крові на ТТГ, Т3, Т4 (за потреби)
- Мікроскопія осаду сечі (обов’язково)
Призначення інструментальних методів обстеження
- ЕКГ (обов’язково)
- УЗДГ серця (за потреби)
- УЗДГ нирок та надниркових залоз (за потреби)
- УЗДГ органів черевної порожнини (обов’язково)
- Фіброеластографія (обов’язково)
- Холангіографія\ холангіопанкреатографія (за потреби)
- РГ ОГК (за потреби)
- СКТ\МРТ ангіографія органів черевновної порожнини (за потреби)
- Біопсія печінки (за потреби)
- Дослідження асцитичної рідини (за потреби)
Встановлення клінічного діагнозу
- Проведення диференційної діагностики
- Встановлення діагнозу токсичний гепатит
- Оцінка та моніторинг ускладнень токсичного гепатиту
- Встановлення супутніх захворювань
Консультації фахівців
- Консультація сімейного лікаря (обов’язково)
- Консультація гастроентеролога (обов’язково)
- Консультація хірурга (за потреби)
- Консультація токсиколога (за потреби)
- Консультація невропатолога (за потреби)
- Консультація офтальмолога (за потреби)
- Консультація реаніматолога (за потреби)
Призначення лікування
- Медикаментозне лікування
- Хірургічне лікування
- Лікування ускладнень
Консультування та підтримка
- Поясніть пацієнту результати діагностичних тестів та встановлену підозру на токсичний гепаптит
- Розкажіть пацієнту про природу захворювання, його можливі причини та перебіг.
- Визначте план регулярного спостереження та контролю симптомів.
- Забезпечте пацієнта інформацією про рекомендований режим дня, раціон харчування та фізичну активність.
- Підкресліть важливість звітування про будь-які зміни в симптомах та ефективності лікування.
- Відповідайте на запитання пацієнта та надавайте підтримку у вигляді посилань на релевантні джерела інформації або підтримуючих груп.
- Обговоріть різні методи лікування, включаючи медикаментозні та хірургічні методи.
- Заплануйте регулярні візити для оцінки ефективності лікування, контролю симптомів та визначення подальших кроків.
Завершення консультації
- Проведіть узагальнення отриманих даних та запитайте пацієнта, чи ніщо важливе не пропущене
- Поінформуйте пацієнта щодо подальшої тактики
- Подякуйте пацієнту
- Утилізуйте ЗІЗ належним чином і помийте руки
Ключові комунікативні навички
Активне слухання
Підбиття підсумків
Виділення вказівних знаків
Початок консультації
- Вимийте руки та при необхідності надіньте ЗІЗ (засоби індивідуального захисту)
- Представтеся пацієнту, вказуючи своє ім’я та посаду
- Підтвердіть прізвище, ім’я, по батькові та дату народження пацієнта
- Поясніть пацієнту мету консультації та процедури, що включатиме обстеження, використовуючи зрозумілу для пацієнта мову.
- Отримайте згоду на консультування та надання медичної допомоги
Запитання
“Ваше прізвище, ім’я та по батькові?”
“Яка дата Вашого народження?”
“Коли Вас було госпіталізовано?”
“Назвіть, будь ласка, Вашу адресу?”
“Хто Ваш сімейний лікар?”
“Чи згодні ви пройти обстеження і лікування у нашій клініці?”
Сьогодні хвороби печінки переважають над усіма захворюваннями органів травлення. З огляду на важливу роль печінки в метаболізмі хімічних речовин можна стверджувати, що не існує ксенобіотиків, які за певних умов не викликали б її ураження. Численні відомості про можливу гепатотоксичну дію різних етіологічних чинників дають змогу дійти висновку, що токсичне ураження печінки – одна з важливих проблем гепатології.
Токсичний гепатит – дифузний запальний процес у печінці, зумовлений впливом речовини з гепатотоксичною дією у дозах, що перевищують гранично допустиму концентрацію (ГДК), який характеризується стеатозом, лімфолейкоцитарною інфільтрацією печінкових часточок і дифузним фіброзом без порушення архітектоніки печінки.
Сьогодні згідно з реєстром LiverTox®, що містить інформацію про підтверджену гепатотоксичність лікарських засобів, відомо більше ніж 1000 медикаментів, біологічно активних добавок (БАД), фітопрепаратів, які викликають медикаментозне ураження печінки (МУП). З кожним роком перелік цих препаратів зростає.
У структурі захворювань печінки частота МУП становить у середньому 5-7%. Як правило, воно пов’язане з використанням протитуберкульозних, антибактеріальних препаратів, анальгетиків, гормональних, цитостатичних, гіпотензивних, антиаритмічних засобів. МУП є основною причиною гострого гепатиту у 30% пацієнтів старших 40 років, фульмінантної печінкової недостатності, яка потребує трансплантації печінки, у 25% випадків, а також у 10% може призвести до смерті.
Істинна поширеність МУП залишається невідомою. Незважаючи на зростання обізнаності про гепатотоксичність препаратів, абсолютна частота реакцій печінки на ліки не знижується. Це зумовлено постійним зростанням асортименту доступних фармакологічних препаратів, широким використанням БАД, захопленням фітопрепаратами, які не проходять належного токсикологічного, радіологічного контролю, клінічних випробувань і приймаються пацієнтом самостійно, без призначення лікаря. Результати досліджень етіології гострої печінкової недостатності показали, що саме лікарські засоби є її основними причинами у США, країнах Європи та Японії. У США та Європі ідіосинкратичні реакції, зумовлені лікарськими засобами, найчастіше стають підставами МУП, тоді як використання традиційних комплементарних і дієтичних добавок є основною причиною МУП у країнах Азії.
Епідеміологія МУП утруднена через проблеми діагностики, встановлення істинного причинно-наслідкового зв’язку, несвоєчасне інформування про випадки МУП, відсутність загальних підходів до їх реєстрації. Важливі фармакоепідеміологічні відомості про МУП були отримані з бази даних досліджень загальної практики (GPRD) у Великобританії. Відповідно до них найбільш частими агентами, що викликають МУП, є антибактеріальні препарати, зокрема флуклоксацилін, еритроміцин, амоксицилін, амоксицилін/клавуланова кислота і ко-тримоксазол, а також диклофенак і протиепілептичні засоби.
За даними Швейцарського реєстру з фармакоепідеміології в стаціонарі, поширеність МУП при госпіталізації була оцінена як 0,7%, а загальна захворюваність під час госпіталізації – 1,4%. Ще більш важливо, що пошкодження печінки не було зазначено в діагнозі в 52-68% випадків. Вивчення GPRD у Великобританії та бази даних шведської гепатологічної клініки показало, що рівень захворюваності на МУП становить 2,3-2,4 на 100 тис. населення на рік.
За результатами проспективного трирічного дослідження, проведеного у Франції, було встановлено, що захворюваність на МУП дорівнює 13,9 на 100 тис. населення, це щонайменше в 16 разів частіше, ніж за даними спонтанних повідомлень за той самий період. Проспективне епідеміологічне дослідження, проведене в Ісландії протягом 2 років, продемонструвало вищу захворюваність на МУП порівняно з Францією: 19 на 100 тис. населення на рік. Незважаючи на те, що амоксицилін/клавуланова кислота використовувалася найчастіше, ризик розвитку МУП спостерігався лише в 1 з 2300 осіб, котрі його застосовували, тоді як найвищий ризик гепатотоксичності був пов’язаний з азатіоприном та інфліксимабом – в 1 з 133 і 148 осіб відповідно. Проспективне загальнонаціональне дослідження, присвячене МУП, проведене у 17 університетських клініках Кореї, дало змогу встановити, що частота госпіталізації через МУП дорівнювала 12 на 100 тис. осіб. Основною причиною гепатотоксичності в Кореї, як і в багатьох інших країнах Азії, було використання різних форм рослинних препаратів [18]. У світі, зокрема Швеції, Іспанії, Ірландії, Франції, створено реєстри для фіксування випадків МУП.
Національними інститутами охорони здоров’я США в 2004 р. ініційовано і фінансується Drug-Induced Liver Injury Network (DILIN) – триваюче обсерваційне дослідження дітей (>2 років) і дорослих з підозрою на МУП. Дослідження, проведені DILIN, зробили важливий внесок у розуміння клінічних, фармакологічних і генетичних аспектів МУП.
Додатково до реєстрів МУП були також розпочаті одноцентрові когортні дослідження в Індії та Туреччині, за даними яких антибіотики та протитуберкульозні препарати є найбільш частими причинами МУП.
За механізмом фармакологічного впливу МУП класифікують на дві групи:
1) індуковані прямим токсичним впливом лікарського препарату на тканину печінки
2) ідіосинкратичні.
Пряму токсичність медикаментів фіксують у значної частини пацієнтів, які зазнали впливу препарату, вона є передбачуваною, розвивається протягом короткого часу (від годин до днів з моменту прийому лікарського засобу) і залежить від дози. Ідіосинкратичний лікарський гепатит, як правило, не пов’язаний з дозою препарату, належить до непередбачуваних реакцій, зумовлених індивідуальними особливостями організму пацієнта. Ураження печінки може мати латентний характер або проявлятися через тривалий час після прийому першої дози і прогресувати незалежно від відміни препарату. Саме ідіосинкратичні реакції становлять більшість випадків МУП, що зумовлює їх важливе клінічне значення і складність медичної проблеми.
До препаратів з прямою гепатотоксичною дією належать ацетамінофен, аміодарон, анаболічні стероїди, антиретровірусні засоби, вальпроєва кислота, циклоспорин, гепарини, холестирамін, нікотинова кислота, статини.
Гепатотоксичність ацетамінофену (парацетамолу) є найбільш поширеною причиною гострої печінкової недостатності (ГПН) у США і деяких країнах Європи. За даними офіційної статистики США, на частку пошкодження парацетамолом припадає 50% випадків ГПН. Половина випадків ГПН, як правило, зумовлена прийомом ацетамінофену протягом декількох днів у добових дозах 4-10 г, хоча за результатами багатоцентрового проспективного дослідження, проведеного у США, ГПН може розвинутися й у разі застосування цього препарату в добових дозах від 2 до 4 г.
Такі чинники, як прийом супутніх препаратів, голодування, системні захворювання та хронічне зловживання алкоголем, впливають на порогову токсичну дозу, діючи на цитохром Р450 (основний фермент, який перетворює ацетамінофен у реактивний метаболіт) або вміст глутатіону (головний фактор детоксикації). Якщо кількість глутатіону в мітохондріях зменшується, токсичний метаболіт ковалентно зв’язується з мітохондріальними білками і викликає збільшення продукції активних форм кисню. Останні призводять до активації протеїнкіназ із подальшим посиленням проникності мембран мітохондрій і вивільненням білків, які пошкоджують ядерну ДНК та при виснаженні АТФ спричиняють некроз гепатоцитів.
Ідіосинкратичну реакцію потенційно може викликати будь-який лікарський засіб, адже вона залежить від генетичних особливостей пацієнта й імунної реактивності організму. Водночас найчастіше зумовлюють персоніфіковану гепатотоксичність алопуринол, аміодарон, амоксицилін/клавуланова кислота, диклофенак, дисульфірам, ізоніазид, кетоконазол, лізиноприл, статини, сульфаніламіди, фенофібрат, контрацептиви, левофлоксацин, фенобарбітал, тамоксифен та ін.
Лікарям загальної практики слід пам’ятати також про потенційну гепатотоксичність фітопрепаратів і харчових добавок. Спостереження останніх десятиліть показали, що рослинні лікарські засоби можуть викликати широкий спектр пошкоджень печінки: від легкого безсимптомного підвищення рівня цитолітичних ферментів до тяжких запально-деструктивних процесів і судинних уражень органа.
Найвищий рівень доказів щодо гепатотоксичності мають препарати самосилу гайового (Teucrium chamaedrys), м’яти болотної (Hedeoma pulegioides), чистотілу (Chelidonium), кава-кава (Piper methysticum), клопогону гроновидного (Actaea racemosa). Доведеною є гепатотоксичність листя креозотового куща (Larrea tridentata), сени (Cassia angustifolia), водно-спиртових екстрактів зеленого чаю і Herbalife.
У деяких реакціях ідіосинкратичного МУП беруть участь ті самі патогенетичні механізми, що і в розвитку прямих гепатотоксичних реакцій: утворення активних форм кисню, мітохондрільна дисфункція та змінений гомеостаз жовчних кислот. Унаслідок пошкодження гепатоцитів ідіосинкратичне МУП запускає запальну реакцію, в яку залучена вроджена імунна система. Основна гіпотеза полягає в тому, що неоантигени стимулюють клітини вродженої імунної системи й ініціюють запалення, зв’язуючись із toll-подібними рецепторами та рецепторами макрофагів. Антигени, отримані з пов’язаних із пошкодженням молекулярних структур (DAMP), діють як сигнали для активації вроджених імунних клітин. Білок групи 1 з високою рухливістю (HMGB1) є одним з раніше ідентифікованих DAMP. HMGB1 індукує інфільтрацію нейтрофілів, зв’язується з toll-подібними рецепторами і сприяє виділенню цитокінів, таких як фактор некрозу пухлини (ФНП), інтерферон-γ й інтерлейкін-1, тим самим активуючи клітини Купфера і посилюючи ідіосинкратичне МУП. Крім того, вивільнення цитокінів і хемокінів може посилювати адаптивну імунну відповідь за допомогою різних механізмів. У процесі метаболізму лікарського засобу його метаболіт ковалентно зв’язується з печінковим білком або модифікованими білками, які експресуються на поверхні гепатоцитів, та утворює білкові гаптени (по суті, неповний антиген). Гаптен вивільняється після загибелі або пошкодження гепатоцитів і представлений антигенпрезентувальними клітинами з молекулами головного комплексу гістосумісності (HLA) класу II у кластері диференціювання CD4+ T-клітин. Коли T-клітини розпізнаються як чужорідні, після зв’язування з T-клітинними рецепторами CD4+ Т-клітини потім активують кластер диференціювання 8 CD8+ Т-цитотоксичних клітин за допомогою секреції ФНП й інтерферону-γ. Цитотоксичні клітини CD8+ T опосередковують цитотоксичні реакції й індукують гепатоцелюлярний апоптоз.
Факторами ризику розвитку МУП вважаються вік і стать пацієнта, етнічна належність, вживання алкоголю, вагітність, наявність поліморбідності, хронічних захворювань печінки, а також властивості лікарських препаратів і генетичні особливості організму пацієнта. Хоча під час старіння організму уповільнюються процеси метаболізму фармакопрепратів, не отримано переконливих даних про те, що похилий вік є фактором ризику МУП. Більше значення в цьому має наявність в осіб похилого віку поліморбідності та зумовлена нею поліпрагмазія. Проте доведений вплив віку на ризик розвитку МУП, спричиненого специфічними агентами. Зокрема, в осіб старших 50 років у 5 разів частіше розвивається МУП, асоційоване із застосуванням ізоніазиду. Вживання вальпроєвої кислоти є фактором ризику розвитку МУП у молодих пацієнтів. Найвищий ризик розвитку гепатоцелюлярного ушкодження мають діти до 10 років, а у дітей молодших 2 років можлива фульмінантна печінкова недостатність з летальним результатом внаслідок відмінності в метаболізмі лікарських засобів і зниження зв’язування білка з плазмою крові.
Епідеміологічні дані з Іспанії, США та Ісландії не засвідчили гендерних відмінностей у розвитку МУП. Етнічну належність слід вважати фактором ризику розвитку МУП. Внаслідок генетично зумовленого зниження активності цитохрому Р450 афроамериканці й латиноамериканці більш чутливі до прийому ізоніазиду. Південно-азіатське походження пацієнтів визнано потенційним фактором ризику ідіосинкратичних МУП, що призводять до фульмінантної печінкової недостатності, яка потребує трансплантації печінки.
Хронічне зловживання алкоголем спричиняє виникнення гепатотоксичних реакцій при нижчих дозах низки препаратів, значно збільшуючи тяжкість таких реакцій при застосуванні парацетамолу, ізоніазиду, нікотинаміду, метотрексату. Інформація про препарати, пов’язані з МУП у вагітних, обмежується в основному антигіпертензивними засобами (метилдопа та гідралазин), тиреостатичними препаратами для блокування синтезу тиреоїдних гормонів при гіперфункції щитоподібної залози (пропілтіоурацил) і протимікробними засобами (зокрема тетрациклін та антиретровірусні препарати).
Вплив супутніх захворювань на розвиток медикаментозно індукованої жирової хвороби печінки був оцінений у контрольованих дослідженнях. Останні дали змогу виявити, що ліки можуть працювати синергічно з іншими факторами ризику, сприяючи розвитку та прогресуванню захворювання печінки. Ожиріння та надлишкова маса тіла виявилися додатковими факторами ризику розвитку МУП. Доведені тригерна роль метотрексату в розвитку стеатогепатиту та фіброзу і вплив хронічного гепатиту В і С на ризик розвитку МУП при використанні антиретровірусної та протитуберкульозної терапії.
Отже, особливості лікарського препарату, зокрема його ліпофільність, доза, тривалість використання, хімічна структура, а також одночасне застосування декількох препаратів (поліпрагмазія) підвищують імовірність розвитку МУП.
З’ясування основних скарг
- Використовуйте відкриті запитання, щоб вивчити скарги пацієнта
- Деталізація основних скарг
Чи відчуваєте Ви біль або неприємні відчуття в області правого верхнього квадранта живота?
Чи помічали Ви зміни в кольорі сечі або калу?
Чи помічали Ви пожовтіння шкіри та\або склер?
Як Ви оцінюєте свій загальний стан?
Чи відчуваєте Ви втому, слабкість або втрату апетиту?
Чи є у Вас скарги на запаморочення, блювоту чи інші симптоми?
Чи турбує Вас біль у суглобах?
Чи турбує Вас печія?
Чи турбує Вас свербіж шкіри?
Чи помічали Ви утворення гематом на Вашому тілі?
Чи помічали Ви збільшення об’єму живота?
Чи Ви вживаєте або вживали ліки, які могли бути причиною даних симптомів?
Чи вживаєте Ви алкоголь або інші токсичні продукти?
Чи були у Вас контакти з токсичними речовинами?
Клініка гепатитів залежить від стадії захворювання та активності процесу. При оцінці скарг виділяють наступні клінічні синдроми.
Больовий синдром: постійний або періодичний біль (іноді відчуття важкості) у правому підребер’ї або епігастральній ділянці, різного характеру та інтенсивності, посилюються після незначного фізичного навантаження, похибок у дієті.
Астено-вегетативний синдром: слабкість, швидка втомлюваність, зниження працездатності, поганий настрій, дратівливість, головний біль, кардіалгії, зниження маси тіла.
Диспепсичний синдром, при якому виділяють:
1) шлункову диспепсію: зниження апетиту, гіркота й сухість у роті, важкість в епігастрії, відрижка, погана переносимість жирної їжі, нудота, іноді блювота;
2) кишкову диспепсію: здуття живота, проноси, закрепи, що нерідко поєднуються зі схудненням, аж до кахексії.
Геморагічний синдром: ламкість судин, геморагії на тілі, легка уразливість ясен, кровотечі (маткові, носові й ін.).
Набряково-асцитичний синдром: збільшення живота (асцит), набряки нижніх кінцівок.
Дисендокринний синдром: зниження лібідо, гінекомастія у чоловіків, аменорея у жінок.
Суглобний синдром: біль у суглобах, їх деформація, утворення анкілозів, біль у м’язах.
Синдром холестаза (недостатнє виділення всіх або основних компонентів жовчі, у першу чергу, жовчних кислот): стійка або нестійка жовтяниця, шкірна сверблячка, особливо вночі, потемніння сечі, знебарвлені випорожнення.
Пропасний синдром: підвищення температури тіла може бути ремітуючим або навіть гектичним, з ознобом і потовиділенням.
Синдром печінкової енцефалопатії: зниження пам’яті, порушення мислення, сонливість, неадекватність поведінки, дезорієнтація в часі й просторі, печінкова кома (найбільш важка стадія печінкової енцефалопатії).
- Проаналізуйте роздуми, побоювання та очікування пацієнта
Ключовим компонентом збору анамнезу є вивчення роздумів, занепокоєнь і очікувань пацієнта, щоб отримати уявлення про те, як пацієнт зараз сприймає свій стан, що його хвилює та чого він очікує від консультації.
Вивчення роздумів, занепокоєнь та очікувань має бути плавним протягом консультації у відповідь на сигнали пацієнта. Це допоможе зробити Вашу консультацію орієнтованою на пацієнта, а не шаблонною.
Використовувати структуру аналізів роздумів, побоювань та очікувань необхідно так, щоб це звучало природно у Вашій консультації.
| Роздуми | Вивчіть уявлення пацієнта щодо поточної проблеми | • «Чи є щось на Вашу думку, що провокує появу або посилення Ваших скарг?» • «Чи можете Ви пов’язати появу Ваших скарг із якоюсь причиною?» |
| Занепокоєння | Вивчіть поточні занепокоєння пацієнта | • «Чи є щось, що Вас турбує?» •«Чи можете Ви пов’язати появу скарг з якоюсь причиною?» •«Як Ви справляєтесь з повсякденною діяльністю?» •«Чи є щось, чого ми з Вами ще не обговорили?» |
| Очікування | Запитайте, що пацієнт сподівається отримати від консультації | • «Чим я можу допомогти Вам сьогодні?» • «Чого Ви очікуєте від сьогоднішньої консультації?» • «Який, на Вашу думку, може бути найкращий план дій?» |
- Резюмуйте скарги пацієнта
Комплексна оцінка включає проведення короткого опитування пацієнта на наявність симптомів ураження інших систем, які можуть мати або не мати відношення до основної скарги. Комплексне дослідження дозволяє також виявити симптоми, про які пацієнт не згадав. Рішення про те, про які симптоми запитати, залежить від поданої скарги та рівня Вашого досвіду. Деякі приклади симптомів, які Ви можете відстежувати по кожній системі, представлені нижче
| Система | Симптоми |
| Загальні прояви | лихоманка, зміна ваги, втома, пітливість, загальна слабкість |
| Респіраторна | задишка, кашель, біль у грудях |
| Серцево-судинна | біль в грудній клітці, задишка, перебої в роботі серця, серцебиття, набряки нижніх кінцівок, підвищення або зниження АТ |
| Шлунково-кишковий тракт | слинотеча, диспепсія, нудота, блювота, дисфагія, біль у животі, порушення випорожнень |
| Сечостатева | Затримка сечі, нетримання сечі |
| Неврологічна | головний біль, дратівливість, плаксивість, зниження настрою, зниження працездатності, втома |
| Опорно-рухова | біль у грудній стінці, біль в кістках, травма |
| Шкіра | висипання, виразки, крововиливи, петехії, синці, геморагії, новоутворення |
Комплексна оцінка
- Проведіть оцінку інших симптомів для отримання комплексної картини
Збір анамнестичних даних
Збір анамнезу захворювання
- З’ясуйте коли вперше з’явилися симптоми хвороби, які були перші ознаки
- З’ясуйте, які симптоми пацієнт має зараз, як вони змінюються протягом часу
- З’ясуйте, чи скаржиться пацієнт на біль у животі
- З’ясуйте, де саме присутній цей біль (в якій ділянці живота)
- З’ясуйте, чи є у пацієнта порушення апетиту
- З’ясуйте, чи є у пацієнта нудота та\або блювання
- З’ясуйте, чи турбує пацієнта загальна слабкість та підвищена стомлюваність
- З’ясуйте, чи змінювався у пацієнта колір шкіри та слизових оболонок
- З’ясуйте, чи змінювався у пацієнта колір сечі та\або калу
- З’ясуйте, чи турбує пацієнта печія
- З’ясуйте, чи турбує пацієнта свербіж шкіри
- З’ясуйте, чи турбує пацієнта біль у суглобах
- З’ясуйте, чи турбує пацієнта наявність гематом на тілі
- З’ясуйте, чи збільшувався у об’ємі живіт пацієнта
- Спитайте чи звертався пацієнт за медичною допомогою, якщо так, то до кого та чим завершилось його звернення, якщо ні, то уточніть чому не звертався; чи приймав пацієнт самостійно або за призначенням лікаря медичні препарати, якщо так, то, чи змінювався характер скарг на тлі лікування
- У випадку госпіталізації з приводу даних скарг, ознайомтесь з випискою з історії хвороби пацієнта, зверніть увагу на встановлений клінічний діагноз, результати проведених лабораторних та/або інструментальних обстежень, проведене лікування та рекомендації після виписки, а також чи дотримувався пацієнт призначеної схеми лікування
- У випадку проведення пацієнту раніше лабораторних та/або інструментальних обстежень з приводу поточних скарг, проаналізуйте їх результати та вкажіть на важливі знахідки
- З’ясуйте, що спонукало пацієнта звернутися за консультацією цього разу
- Виключіть інші причини наявних скарг, ставлячи пацієнту уточнюючі питання.
Коли у Вас вперше з’явилися симптоми хвороби? Які були перші ознаки?
Які симптоми Ви спостерігаєте зараз? Як вони змінюються протягом часу?
Які симптоми найбільше впливають на Ваше щоденне функціонування?
Чи є певні фактори або ситуації, що можуть погіршити Ваші симптоми?
Як переносили Ви вірусні гепатити або інші захворювання шлунково-кишкового тракту?
Ви звертались за медичною допомогою?
Якими ліками Ви лікуєтеся в даний момент?
Чи впливають ліки на Ваші щоденні активності і як Ви себе відчуваєте під час лікування?
Скажіть, будь ласка, що спонукало Вас звернутися цього разу до мене?
Чи переносили Ви якісь інфекційні захворювання до появи Ваших симптомів?
Чи були у Вас травми та/або оперативні втручання?
Чи спостерігалися у Ваших кровних родичів подібні симптоми?
Чи маєте Ви алергічну реакцію або непереносимість до певних лікарських препаратів?
Чи призначено Вам ліки або терапію для контролю симптомів? Як вони допомагають?
Чи спостерігається у Вас будь-яка реакція на ліки або які-небудь побічні ефекти?
Чи змінились Ваші звичні соціальні або розважальні активності через хворобу?
Збір анамнезу життя
- З’ясуйте наявність у хворого хронічних захворювань, зокрема неврологічних, ендокринних захворювань, захворювань шлунково-кишкового тракту чи нирок тощо
- Уточніть перенесені пацієнтом інфекційні захворювання
- Уточніть, чи проводились пацієнту раніше оперативні втручання
- З’ясуйте, чи були вагітності, роди або кесарів розтин, чи є зараз грудне вигодовування
- З’ясуйте час настання менопаузи та прийом замісної гормональної терапії
- З’ясуйте, чи приймає пацієнт постійно лікарські препарати та які саме, вкажіть дози препаратів
- Уточніть, чи переносив пацієнт раніше травми, з’ясуйте, як протікав відновлювальний період
- З’ясуйте чи є у пацієнта непереносимість лікарських препаратів або продуктів харчування та уточніть, як саме вона проявляється
- Уточніть, чи є у пацієнта шкідливі звички-вживання алкоголю, наркотичних речовин, паління
- З’ясуйте рівень фізичної активності пацієнта
- З’ясуйте сімейний стан пацієнта, побутові умови проживання; уточніть, чи не було серед кровних родичів випадків міастенії та/або інших захворювань, що проявлялися м’язовою слабкістю
- З’ясуйте, чи працює пацієнт, його професію, умови роботи, наявність шкідливих факторів
Фізикальне обстеження
Оцінка загального стану пацієнта
- Проведення загального огляду
- Оцінка конституції
- Оцінка ступеня вгодованості
- Окружність талії
- Шкіра
- Слизові оболонки
- Щитоподібна залоза
- Оцінка периферійних лімфовузлів
- Оцінка органів дихання
- Оцінка серцево-судинної системи
- Оцінка органів черевної порожнини
- Оцінка органів сечостатевої системи
Загальний стан від відносно задовільного до важкого (залежить від стадії та активності процесу).
Свідомість: не порушена, порушена (ейфорія, марення, печінкова кома при інтоксикації центральної нервової системи).
Положення: активне, пасивне (при комі).
Зовнішній вигляд (habitus) – хворий виглядає старше паспортного віку, особливо при гепатитах алкогольного ґенезу.
Шкіра та слизові оболонки: блідість шкіри із сіруватим відтінком, локальна або дифузійна гіперпігментація спостерігається при хронічних захворюваннях печінки, виражена блідість, обумовлена гемолітичною або постгеморагічною анемією – при цирозах печінки.
Жовтяниця – раніше за все її виявляють на склерах і слизовій оболонці м’якого піднебіння, іноді – в ділянці носо-губного трикутника, чола, долонь. При інтенсивній жовтяниці колір шкіри може стати зеленувато-жовтим через окислення білірубіну в білівердин. Іноді може бути відсутня.
Розчухи на шкірі, що є результатом інтенсивної шкірної сверблячки, обумовленої подразненням нервових закінчень шкіри жовчними кислотами, порушенням жовчовиділення при розвитку холестаза. Сверблячка може виникати й при відсутності жовтяниці.
“Печінкові долоні” (гіперемія тенора й гіпотенара), “печінковий язик” (малиновий), “судинні зірочки” (телеангіектазії або зірчасті ангіоми, що представляють собою утворення, які піднімаються над шкірою, від 1мм до 1-2см, що нагадують зірочки, найчастіше розташовуються на шиї, обличчі, плечах, спині, кистях, при натисненні яких предметним склом можна побачити їхню пульсацію) – шкірні симптоми, обумовлені розширенням підшкірних судин під впливом надлишкової кількості естрогенів у крові й зміни чутливості рецепторів.
Геморагічний синдром у вигляді петехій, синців, крововиливів – прояви геморагічного діатезу, що спостерігаються при важкому ураженні печінкової паренхіми.
Ксантоми – внутрішньо шкірні бляшки, що найчастіше розташовуються на повіках (ксантелазми), кистях рук, ліктях, колінах, стопах, сідницях, у пахвових ділянках, походження яких пов’язане з підвищеним вмістом у крові ліпідів.
«Малиновий язик», випадання волосся у пахвових ділянках і на лобку характерні для хронічних захворювань печінки.
Білі нігті при хронічному захворюванні печінки обумовлені порушенням обміну й накопиченням естрогенів і серотоніну.
Атрофія м’язів плечового поясу, обумовлена порушенням білкового обміну й гормональним дисбалансом.
«Барабанні палички» – стовщення дистальних фаланг пальців рук, обумовлене вираженою диспротеінемією.
Припухлість суглобів («міліарний ревматизм») спостерігається, головним чином, при міліарному цирозі печінки.
Ендокринні порушення:
– гінекомастія та жіночий тип оволосіння шкірних покривів, атрофія яєчок у чоловіків, пов’язані з гіперіестрогенемією, спостерігаються при важкому ураженні печінки;
– випадання волосся на лобку й аксилярних ділянках, гіпертрофія навколо вушних слинних залоз – при алкогольних гепатопатіях;
– інфантильність (недорозвинення вторинних статевих ознак) спостерігається при хронічних захворюваннях печінки, що розвиваються в дитячому або юнацькому віці, обумовлених порушенням синтезу стероїдних гормонів.
Набряки нижніх кінцівок, лімфоаденопатія, у результаті порушення білкового обміну. Може з’явитися асцит (накопичення рідини в черевній порожнині), у результаті як вираженої гіпоальбунемії, так і розвитку портальної гіпертензії з ураженням паренхіми печінки.
Гепатомегалія– збільшення розмірів печінки, викликане інфільтрацією паренхіми іммунокомпетентними клітками, холестазом, порушенням кровообігу в системі портальної вени. При огляді живота іноді відзначається асиметрія в епігастральній ділянці, за рахунок зміщення догори правої реберної дуги, велике пухлино подібне вибухання в правому підребер’ї, що зміщується під час дихання. При перкусії печінки відзначається зміщення нижнього краю печінки на 1-6см нижче краю реберної дуги по всіх лініях, при збільшенні лівої частки – зміщення лівої межі на 1-3см назовні від лівої парастернальної лінії. При пальпації печінки нижній край ущільнений, загострений, болісний через розтягання фіброзної капсули, поверхня печінки гладка. Прогресивне зменшення розмірів печінки є несприятливою прогностичною ознакою.
Спленомегалія спостерігається в10-25% хворих гепатитом. Збільшення незначне – 1-2 см.
Оцінка пацієнта за шкалами
- Оцінка термінальної стадії захворювання печінки MELD (за потреби) https://clincasequest.academy/meld-score/ (за потреби)
- Визначення R-значення для оцінки типу ураження печінки. https://clincasequest.academy/r-value/ (за потреби)
- Шкала Чайлд-П’ю для оцінки смертності від цирозу печінки https://clincasequest.academy/child-pugh-score/ (за потреби)
- Шкала RUCAM для оцінки ймовірності медикаментозного ураження печінки DILI/HILI (за потреби)
Призначення лабораторного обстеження
- Загальний аналіз крові (обов’язково)
- Аналіз крові на електроліти (калій, кальцій, натрій) (обов’язково)
- Аналіз крові білкових фракцій крові (обов’язково)
- Аналіз крові на рівень глюкози натщесерце (обов’язково)
- Аналіз крові на печінкові проби (обов’язково)
- Аналіз крові на ліпідний спектр (обов’язково)
- Аналіз крові на ниркові проби (обов’язково)
- Аналіз крові на рівень заліза (за потреби)
- Аналіз крові на рівень вітаміну В12 (за потреби)
- Імунологічне дослідження крові (обов’язково)
- Імуноферентне дослідження та ПЛР маркери вірусних гепатитів (вірусні гепатити А,В,С,Е, викликані вірусом Епштейна-Барр, цитомегаловірусом, вірусом гересу) (обов’язково)
- Тест Фібромакс ™ (FibroMax, FM) (обов’язково)
- Тест на антинуклеарні антитіла (за потреби)
- Аналіз крові на рівень міді (за потреби)
- Аналіз крові на церулоплазмін (за потреби)
- Аналіз сечі на рівень міді (за потреби)
- Коагулограмма (обов’язково)
- Аналіз крові на ТТГ, Т3, Т4 (за потреби)
- Мікроскопія осаду сечі (обов’язково)
Загальний (клінічний) аналіз крові відображає ознаки мезенхімального запалення, для якого характерні:
– лейкоцитоз;
– прискорення ШОЕ;
– еозинофілія;
– підвищення вмісту в крові тромбоцитів;
– білірубін і уробіліногенові тіла.
Мікроскопія осаду сечі проявляється «сечовим синдромом», що обумовлений порушенням ниркової гемодинаміки:
– мікрогематурія;
– помірна протеїнурія;
– лейкоцитурія;
– циліндрурія.
Біохімічне дослідження
- • Синдром цитолізу – підвищення вмісту в крові внутрішньоклітинних ферментів, що відображають важкість запального процесу в печінці:
– трансамінази(АлАТ, АсАТ)
– дегідрогенази (глутаматдегідрогеназа (ГДГ), лактатдегідрогеназа (ЛДГ);
– урокінази;
– підвищення рівня заліза й вітаміну В12 у сироватці крові.
• Синдром холестаза – порушення синтезу, секреції або відтоку жовчі, що не є аналогом жовтяниці. Спостерігається при запальних і пухлинних захворюваннях гепатобіліарної системи й пов’язаний з накопиченням у сироватці крові речовин, що зазвичай екстрагуються жовчу:
– індикаторних ферментів холестаза (лужна фосфатаза, гамма-глутамінтранспептидаза (γ-ГТП), 5-нуклеотидаза, лейцинамінопептидаза (ЛАП);
– загального білірубіну за рахунок кон’югованої фракції (прямої);
– жовчних кислот;
Холестаз може супроводжуватися підвищенням рівня холестерину в сироватці крові. Трансамінази сироватки крові можуть бути нормальними, помірно або значно підвищеними.
• Синдром імунного запалення проявляється підвищенням у сироватці крові:
– вмістузагального білка за рахунок глобулінів, особливо β- і γ-глобулінів;
– рівня імуноглобулінів А, М, G;
– появою позитивних осадових проб (тимолової, формолової, сулемової).
• Синдром гепатоцелюлярної недостатності (3 стадії: початкова, стадія компенсації, стадія вираженої декомпенсації), що проявляється:
– зниженням рівня ферментів, які синтезуються в печінці (трансамінази, альдолази, оксидази);
- – збільшенням рівня некон’гованого білірубіну;
- – зниженням вмісту в крові загального білка, альбумінів (гіпоальбумінемія), факторів згортання крові;
- – відносною гіперальдостеронемією;
- – гіпокаліємією;
- – зміною кислотно-лужної рівноваги.
- • Синдром ниркової недостатності, обумовлений зниженням ниркового кровотоку, кортикальної перфузії, клуб очкової фільтрації, що проявляється:
- – зниженням концентраційної функції;
- –підвищенням концентрації в крові сечовини, креатиніну;
- –електролітним дисбалансом.
- Фібромакс ™ (FibroMax, FM) – це комплекс розрахункових тестів (математична модель) для визначення ступеня гістологічної активності при найбільш поширених формах патології печінки. Діагностика проводиться без біопсії, для розрахунку використовуються результати спеціальних досліджень крові (біохімічних аналізів) і мінімальні анамнестичні дані про пацієнта.
- Фібромакс – комплекс розрахункових показників для оцінки ступеня фіброзу, стеатозу та активності патологічного процесу в печінці, що дозволяє встановити п’ять найважливіших показників стану тканини печінки, а саме:
- A. Стадія фіброзу за шкалою METAVIR (ФіброТест).
- B. Ступінь некрозапальної активності (АктиТест).
- C. Ступінь стеатозу (жирового переродження тканини) печінки (СтеатоТест).
- D. Діагностика неалкогольного пошкодження печінки з визначенням його активності – неалкогольний стеатогепатит (НешТест).
- E. Діагностика алкогольного ушкодження печінки з визначенням його активності (АшТест).
- Таким чином тест ФіброМакс складається з 5 розрахункових алгоритмів і виконується за результатами математичної обробки десяти біохімічних показників крові: альфа2 макроглобулін, гаптоглобін, аполіпопротеїн А1, ГГТ (гамма глютамілтрансферази), загальний білірубін, АЛТ (аланін амінотрансфераза), АСТ (аспарат амінотрансфераза), тригліцериди , загальний холестерин і глюкоза.
- У січні 2007 року Французьке міністерство охорони здоров’я визнало ФіброТест реальною альтернативою біопсії печінки. Це послужило приводом до одночасного впровадження тестів у США, Канаді, Великобританії, Україні та інших країнах. ФіброТест дозволяє отримати точну кількісну та якісну оцінку фіброзу і некрозапальних змін у печінці на всіх стадіях незалежно від локалізації в 95 – 99% випадків, що виключає можливість помилки при локальному дослідженні матеріалу, отриманого методом пункційної біопсії.
- У січні 2008 року Міністерство охорони здоров’я Франції затвердило ФіброТест в якості обов’язкової достовірної неінвазивної методики діагностики гепатиту С в прогресуючій стадії. ФіброТест є єдиним методом подібного роду, який підтриманий і підтверджений більш ніж 40 міжнародними клінічними дослідженнями, опублікованими в провідних наукових журналах по всьому світу.
- Фібромакс – комплекс розрахункових показників для оцінки ступеня фіброзу, стеатозу та активності патологічного процесу в печінці, що дозволяє встановити п’ять найважливіших показників стану тканини печінки, а саме:
- Фібромакс ™ (FibroMax, FM) – це комплекс розрахункових тестів (математична модель) для визначення ступеня гістологічної активності при найбільш поширених формах патології печінки. Діагностика проводиться без біопсії, для розрахунку використовуються результати спеціальних досліджень крові (біохімічних аналізів) і мінімальні анамнестичні дані про пацієнта.
Призначення інструментальних методів обстеження
- ЕКГ (обов’язково)
- УЗДГ серця (за потреби)
- УЗДГ нирок та надниркових залоз (за потреби)
- УЗДГ органів черевної порожнини (обов’язково)
- Фіброеластографія (обов’язково)
- Холангіографія\ холангіопанкреатографія (за потреби)
- РГ ОГК (за потреби)
- СКТ\МРТ ангіографія органів черевновної порожнини (за потреби)
- Біопсія печінки (за потреби)
- Дослідження асцитичної рідини (за потреби)
У пацієнтів із гострим токсичним гепатитом зазвичай не має суттєвих змін при візуалізації або діагностується лише легка гепатомегалія.
У пацієнтів із медикаментозною гострою печінковою недостатністю може зменшуватися об’єм печінки в міру прогресування захворювання. Пацієнти з хронічним токсичним гепатитом зазвичай не мають суттєво розширених внутрішньо- та позапечінкових жовчних протоків, але у деяких випадках можуть спостерігатися цирозу, спленомегалія та збільшений внутрішній діаметр ворітної вени.
Візуалізаційні дослідження часто допомагають діагностувати синдром синусоїдальної обструкції або веноокклюзійне захворювання печінки, звичайна комп’ютерна томографія (КТ) може виявити набряк печінки, а розширене СКТ ангіографічне дослідження може виявити нерівномірні або часткові зміни зображень печінки, розмиті печінкові вени та асцит.
Звичайні візуалізаційні дослідження, включаючи ультразвукове дослідження, КТ або МРТ, а також ретроградна холангіопанкреатографія мають велике значення для диференціальної діагностики холестатичного токсичного гепатиту від причин обструкції жовчних шляхів, таких як жовчно-кам’яна хвороба, злоякісні новоутворення підшлункової залози або жовчних шляхів.
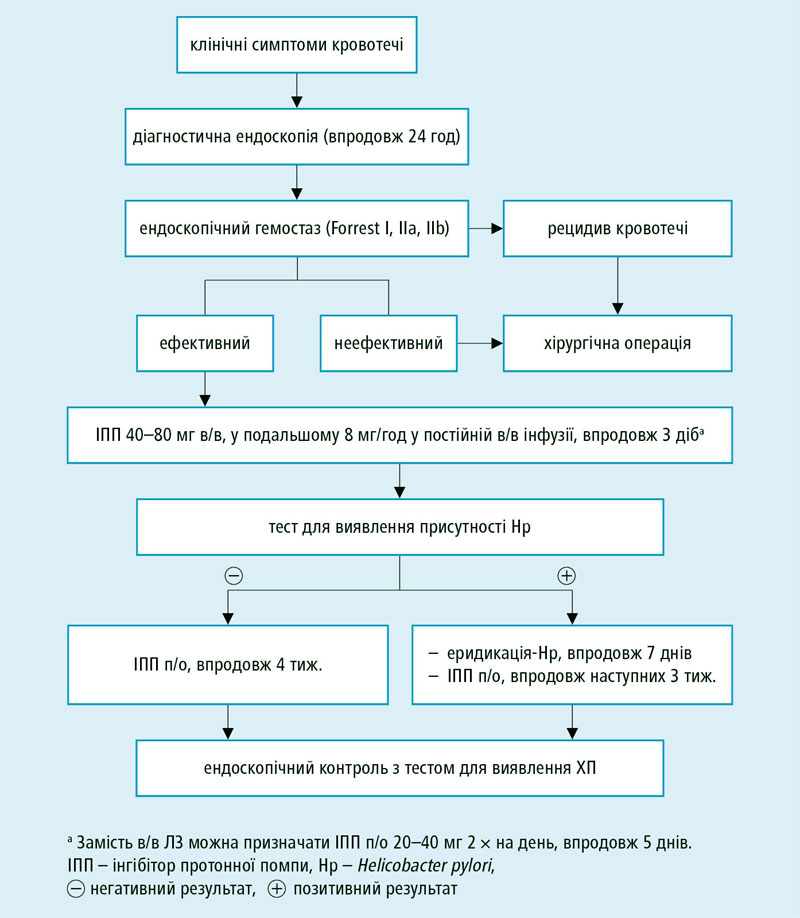
Якщо серія клінічних досліджень і лабораторних тестів все ще не допомагають встановити діагноз токсичний гепатитI, біопсія печінки може бути корисною для діагностики та оцінки тяжкості ураження печінки.
Біопсію печінки слід розглянути, якщо виконується будь-який із наступних пунктів:
- діагноз токсичний гепатит залишається невизначеним після того, як відповідні лабораторні тести не виявили етіології, і особливо, коли не можна виключити автоімунний гепатит;
- при зупинці прийому гепатотоксичних препаратів, рівні печінкових біохімічних показників продовжують погіршуватися або з’являються інші ознаки погіршення функції печінки;
- рівні біохімічних показників печінки не знижуються до ≤50% від пікових значень після припинення прийому підозрілого препарату протягом 1–3 місяців;
- підозра на наявність хронічного токсичного гепатиту або іншого супутнього хронічного захворювання печінки;
- тривале застосування певних препаратів, які можуть спричинити фіброз печінки, наприклад, метотрексат.
Встановлення клінічного діагнозу
- Проведення диференційної діагностики
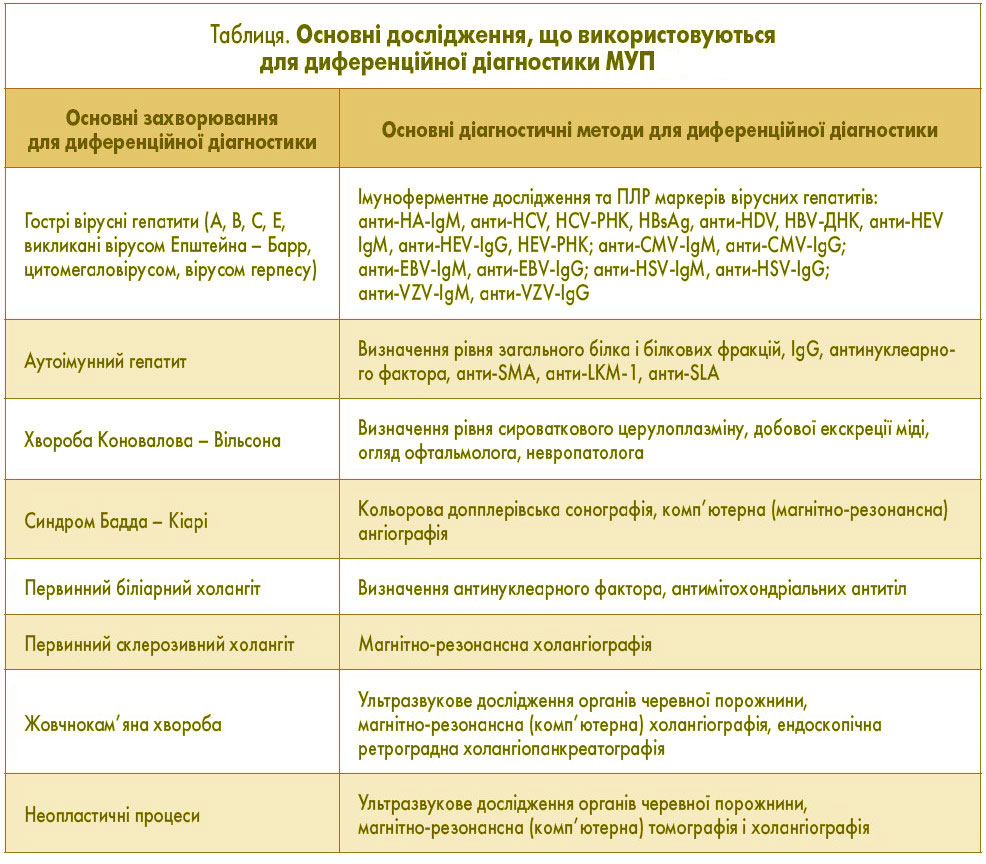
Токсичний гепатит має складні клінічні фенотипи, які охоплюють майже всі відомі фенотипи гострого, підгострого та хронічного ураження печінки. Таким чином, слід виключити будь-які інші гепатобіліарні захворювання, включаючи всі типи вірусного гепатиту (особливо спорадичний гепатит Е), шляхом детального обстеження.
| Захворювання, з якими проводять диференційну діагностику ТГ | Ключові діагностичні параметри |
| Вірус гепатиту А (HAV) | Сироватковий анти-HAV-IgM |
| Вірус гепатиту B (HBV) | Сироватковий поверхневий антиген HBV (HBsAg), анти-HBc-IgM; HBV ДНК (PCR) |
| Вірус гепатиту С (HCV) | Сироватковий анти-HCV, антиген HCV; РНК HCV (RT-PCR) |
| Вірус гепатиту Е (HEV) | Сироватковий анти-HEV-IgM, підвищення титру анти-HEV-IgG; РНК HEV (RT-PCR) |
| Цитомегаловірус (ЦМВ) | Сироваткові анти-CMV-IgM, підвищення титру анти-CMV-IgG; ДНК ЦМВ (ПЛР) |
| Вірус Епштейна-Барр (EBV) | Сироваткові анти-EBV-IgM, підвищення титру анти-EBV-IgG; ДНК EBV (ПЛР) |
| Вірус простого герпесу (ВПГ) | Сироватковий анти-HSV-IgM, підвищення титру для anti-HSV-IgG; ДНК HSV (ПЛР) |
| Вірус вітряної віспи (VZV) | Сироваткові анти-VZV-IgM, підвищення титру анти-VZV-IgG; РНК VZV (RT-PCR) |
| Інші вірусні інфекції | Сироваткові специфічні біомаркери аденовірусу, вірусу Коксакі-В, еховірусу, вірусу кору, вірусу краснухи тощо |
| Алкогольна хвороба печінки | Історія зловживання алкоголем. АСТ/АЛТ сироватки >2, ГГТ > ВМН |
| Неалкогольна жирова хвороба печінки | Індекс маси тіла, інсулінорезистентність, гепатомегалія, ехогенність печінки |
| Аутоімунний гепатит | γ-глобуліни, ANA, SMA, анти-LSP, анти-ASGPR, анти-LKM |
| Первинний біліарний холангіт | AMA, анти-PDH-E2. Гістопатологія печінки |
| Первинний склерозуючий холангіт | p-ANCA, MRC. Гістопатологія печінки |
| Аутоімунний холангіт | АНА, СМА. Гістопатологія печінки |
| Жовчні захворювання | Механічна жовтяниця, підвищення сироваткових ЩФ і ГГТ; холангіектази та запалення, спричинені конкрементами жовчної протоки або іншими факторами. Зазвичай потрібна сонографія гепатобіліарної системи. |
| хвороба Вільсона | Генотипування хвороби Вільсона; зниження сироваткового церулоплазміну; підвищення вільної міді в сироватці крові; кільце Кайзера–Флейшера; неврологічно-психіатрична аномалія |
| Гемохроматоз | Генетичне тестування. Підвищене насичення трансферину та рівень феритину. Біопсія печінки для оцінки концентрації заліза в печінці та ступеня ураження печінки |
| Дефіцит альфа-1 антитрипсину | Зниження рівня α1-антитрипсину в сироватці крові, аномальна рухливість аномальної молекули α1-AT при ізоелектричному фокусуванні |
| Токсичне захворювання печінки | Скринінг на побутові, професійні та інші токсини |
| Сепсис і септичний шок | Підрахунок і сортування лейкоцитів, бактеріальний посів крові чи іншого зразка |
| Серцево-судинне захворювання | Ехокардіограма, електрокардіограма та клінічний контекст для виявлення будь-яких серцево-судинних захворювань, що призводять до гіпотензії або шоку. Допплерографія для виявлення тромбозу |
| Захворювання легень | КТ і клінічний контекст для виявлення інфаркту легені, ХОЗЛ або інших захворювань легенів |
| захворювання щитовидної залози | Базальний ТТГ, Т3, Т4, вільний Т3, вільний Т4, тиреоїдні аутоімунні антитіла |
| Ревматичні захворювання | Опорно-руховий апарат і шкіра в анамнезі та клінічні особливості. Ревматичний фактор і аутоімунні антитіла. Рентгенографія, КТ та МРТ |
| Інший статус | Лімфома та інші онкологічні захворювання; Хвороба Аддісона (кортизол плазми); парентеральне харчування; політравма; великі судомні напади; сильні фізичні навантаження та ін |
Для пацієнтів, які отримують хіміотерапевтичні або імуносупресивні методи лікування та мають позитивні маркери HBV або HCV, якщо у них є дисфункція печінки або гостре ураження печінки, слід визначити, чи це спричинено реактивацією вірусу, хіміотерапевтичними/імуносупресивними засобами, чи одночасним впливом обох чинників. Для пацієнтів зі СНІДом, які отримують антиретровірусну терапію (АРТ), якщо вони мають одночасно позитивні маркери HBV або HCV та ураження печінки, слід визначити, чи спричинене ураження печінки АРТ чи реактивацією вірусу гепатиту.
Крім того, слід також виключити ураження печінки внаслідок сепсису, отруєння, серцевої недостатності, гіпотонії або шоку, оклюзії судин і легеневої недостатності. Слід зазначити, що асцит може бути початковим клінічним проявом синдрома синусоїдальної обструкції / веноокклюзійного захворювання печінки.
Ознаки деяких пацієнтів із токсичними гепатитами схожі на клінічні ознаки пацієнтів з класичним автоімунним гепатитом. У таких пацієнтів можуть визначатися відповідні автоантитіла, пов’язані з ураженням печінки, і вони можуть реагувати на терапію стероїдами. Таким чином, клінічно важко відрізнити ТГ від автоімунних гепатитів у цих пацієнтів. Загалом слід звернути особливу увагу на автоімунні гепатити, що виникають на фоні токсичного ураження печінки.
Автоімунно-токсичні гепатити є найчастішим явищем у вищезазначених трьох контекстах, і при цьому стані ураження печінки зазвичай супроводжується значним підвищенням рівня імуноглобуліну в сироватці крові та наявністю антинуклеарних антитіл (ANA), антитіл до гладкої мускулатури (ASMA), антитіл до печінки та нирок, мікросомне антитіло-1 (анти-LKM-1), а іноді і антимітохондріальне антитіло (AMA). Такі пацієнти зазвичай мають хронічний перебіг і симптоми, подібні до автоімунного гепатиту, що можуть прогресувати. Пацієнти з автоімунно-токсичними гепатитами зазвичай добре реагують на терапію глюкокортикоїдами без рецидивів ураження печінки.
Гістопатологічні ознаки класичного автоімунного гепатиту включають інфільтрацію плазматичними клітинами, розеткоподібні зміни гепатоцитів і емпериполез лімфоцитів, тоді як автоімунно-токсичні гепатити можуть мати інфільтрацію нейтрофілів і еозинофілів у портальній зоні, а також гепатоцелюлярний холестаз.
Для пацієнтів, у яких ураження печінки виникло вперше, з певним анамнезом прийому ліків і вираженими автоімунними ознаками, лікування глюкокортикоїдами можна розглядати після відміни підозрюваних токсичних препаратів, і якщо хімічні показники печінки не покращуються.
Після одужання пацієнта дозу глюкокортикоїдів слід поступово знижувати до повної відміни. Якщо на етапі спостереження немає ознак рецидиву, то ймовірність встановлення діагнозу токсичного гепатиту зростає. В іншому випадку слід розглядати діагноз класичного автоімунного гепатиту.
- Встановлення діагнозу токсичний гепатит (ТГ)
Встановлення діагнозу ТГ передбачає виключення будь-якої іншої причини, здатної викликати ураження печінки (алкоголь, віруси, аутоімунні, холестатичні, метаболічні захворювання і гемодинамічні розлади). Біопсія печінки не є обов’язковою в діагностиці ТГ, особливо тоді, коли доведена гепатотоксичність відомого раніше медичного препарату.
Діагностика ТГ у більшості випадків є складною, особливо у пацієнтів, які мають дифузне ураження печінки. Цей факт вимагає від лікаря ретельного збору анамнезу, гарної орієнтації в клінічних і морфологічних проявах ураження. При встановленні діагнозу ТГ необхідно враховувати основні етапи:
1. Ретельний збір анамнезу захворювання пацієнта: які приймає ліки пацієнт зараз; тривалість прийому та доза; з’ясувати можливе їх використання пацієнтом у минулому.
2. Оцінка часового зв’язку виявлених клініко-лабораторних синдромів, що характеризують ТГ, з прийомом лікарського препарату.
3. Оцінка динаміки виявлених клініко-лабораторних синдромів, що характеризують ТГ, з відміною лікарського препарату.
4. Виключення інших можливих причин пошкодження печінки (вірусні гепатити, аутоімунний гепатит, механічна жовтяниця, первинний склерозуючий холангіт, гранулематоз).
5. Ретельна оцінка стану хворого після повторного прийому препарату.
6. Оцінка морфологічного дослідження печінкового біоптату має обмежене значення для диференційної діагностики ТГ, оскільки існує широкий спектр гістологічних змін, що виникають під впливом ліків, схожих із пошкодженням печінки іншої етіології.
Критерії оцінки медикаментозного ураження печінки (Guidelines in the Recognition and Prevention of Hepatotoxicity in Clinical Practic, 2001):
1. Часовий інтервал між прийомом препарату і розвитком гепатотоксичної реакції: можливий — 5–90 днів; сумнівний — ≥90 днів.
2. Виключення альтернативної причини ТГ шляхом ретельного обстеження.
3. Перебіг реакції після відміни препарату: «можливий ТГ» — зниження рівня печінкових ферментів на 50% від вихідного протягом 8 днів; «сумнівний ТГ» — зниження рівня печінкових ферментів на 50% протягом 30 днів — для гепатоцелюлярного і 180 днів — для холестатичного ураження печінки.
4. Позитивна відповідь на повторне введення препарату — підвищення рівня ферментів у ≥2 разів.
Оцінку ступеня пошкодження печінки може бути проведено за допомогою критеріїв загальної токсичності Національного інституту раку США (US National Cancer Institute), версія 5.0. Крім цих параметрів, необхідне проведення ультразвукового дослідження черевної порожнини або комп’ютерної томографії для оцінки стану жовчовивідних шляхів, судин, оцінки паренхіми печінки та локалізації пухлини. Біопсія печінки не має діагностичного значення при ТГ.
Оцінка ступеня гепатотоксичності згідно з рекомендаціями Національного інституту раку США — NCCN CTC v 5.0
| Показник | Ступінь | ||||
| 0 | I | II | III | IV | |
| ЛФ, разів | Норма | >2,5 × ВМН | >2,5–5,0 × ВМН | >5,0–20,0 × ВМН | >20,0 × ВМН |
| Білірубін, разів | Норма | 1,0–1,5 × ВМН | >1,5–3,0 × ВМН | >3,0–10,0 × ВМН | >10,0 × ВМН |
| ГГТ (γ-глутамінтрансфераза), разів | Норма | >2,5 × ВМН | >2,5–5,0 × ВМН | >5,0–20,0 × ВМН | >20,0 × ВМН |
| АлАТ, разів | Норма | >2,5 × ВМН | >2,5–5,0 × ВМН | >5,0–20,0 × ВМН | >20,0 × ВМН |
| АсАТ, разів | Норма | >2,5 × ВМН | >2,5–5,0 × ВМН | >5,0–20,0 × ВМН | >20,0 × ВМН |
| Гіпоальбумінемія, г/дл | Норма | <3,0 НМН | ≥2,0–<3,0 | <2,0 | – |
| Печінкова дисфункція/недостатність (клінічна) | Норма | – | – | Тремор | Енцефалопатія або кома |
| Стан портальної вени | Норма | – | Зниження кровообігу в портальній вені | Відновлення/ ретроградний потік у портальній вені | – |
Радою міжнародних організацій медичних наук (Council for International Organizations of Medical Sciences – CIOMS) виділені 3 типи ідіосинкратичних МУП: гепатоцелюлярний, холестатичний і змішаний.
Для гепатоцелюлярного типу МУП характерне підвищення рівня аланінамінотрансферази (АЛТ) більше ніж у 2 рази від верхньої межі норми (ВМН), нормальний рівень лужної фосфатази (ЛФ) та коефіцієнт R (співвідношення рівнів АЛТ і ЛФ) ≥5.
Якщо рівень АЛТ перебуває в межах нормальних значень, а рівень ЛФ сягає більше 2 ВМН при індексі R ≤2, діагностують холестатичний тип МУП.
Змішаний тип МУП характеризується підвищенням рівнів АЛТ та ЛФ більш ніж у 2 рази та індексом R=2-5.
Крім ідіосинкратичних, з клінічної точки зору виділяють специфічні фенотипи МУП:
- реакція на медикаменти з еозинофілією та системними симптомами (DRESS-синдром) – індукована лікарськими засобами гіперчутливість із залученням кількох органів і системними проявами, асоційована з прийомом протисудомних препаратів, алопуринолу, міноцикліну, синтетичних противірусних засобів із групи ненуклеозидних інгібіторів зворотної транскриптази;
- аутоімунний гепатит, індукований медикаментами, – гостре МУП із серологічними та/або гістологічними маркерами ідіопатичного аутоімунного гепатиту, асоційоване з прийомом диклофенаку, галотану, індометацину, інфліксимабу, метилдопи, міноцикліну, нітрофурантоїну та статинів;
- холестатичні ураження печінки (вторинний склерозивний холангіт, дуктопенічний синдром) – наявність гістологічних ознак, характерних для первинного склерозивного холангіту, хронічний холестаз, асоційований із втратою жовчних проток, зумовлені прийомом азатіоприну, андрогенів, амоксициліну/клавуланової кислоти, еритроміцину, естрадіолу, карбамазепіну, аміодарону, 6-меркаптопурину, інфліксимабу;
- гостра жирова дистрофія печінки – клінічний синдром зі швидким розвитком печінкової та органної недостатності, пов’язаний із поширеним мікровезикулярним стеатозом. До препаратів, що викликають цей вид МУП, належать аміодарон, противірусні засоби (диданозин, ставудин, зальцитабін) і вальпроєва кислота;
- стеатоз та стеатогепатит – неалкогольна жирова хвороба печінки, яку можна пов’язати із впливом специфічних препаратів, зокрема, метотрексату, 5-фторурацилу, кортикостероїдів, протизаплідних і протипухлинних засобів;
- вузлова регенеративна гіперплазія – дифузне утворення вузликів у центрі та на периферії гепатоцитів унаслідок прийому цитостатичних і протипухлинних препаратів (азатіоприну, бусульфану, блеоміцину, циклофосфаміду, хлорамбуцилу, цитарабіну, кармустину);
- пухлини печінки – гепатоцелюлярна аденома або карцинома, встановлена за допомогою гістологічного дослідження, комп’ютерної чи магнітно-резонансної томографії. Причиною неопластичних новоутворень печінки стає використання анаболічних андрогенних стероїдів і пероральних контрацептивів.
- Оцінка та моніторинг ускладнень токсичного гепатиту
Цироз печінки – прогресуюче поліетіологічнедифузійне хронічне захворювання печінки, що характеризується значним зниженням маси функціонуючих гепатоцитів, вираженим фіброзом з порушенням структури печінкової часточки й судинної системи печінки. Смертність від цирозу печінки в розвинених країнах коливається від 13 до 80 на 100 000 населення.
Класифікація цирозів печінки
За етіологією:
- вірусні (В, С, Д);
- алкогольні;
- токсичні, у тому числі медикаментозні;
- неалкогольний стеатогепатит;
- хвороба Вільсона-Коновалова;
- внаслідок дефіциту α-1-антитрипсину;
- первинний біліарний цироз;
- вторинний біліарний цироз.
- За морфологією:
- дрібновузловий (діаметр вузлів від 1 до 3 мм);
- крупновузловий (діаметр вузлів більш 3 мм);
- змішаний;
- неповний септальний.
За перебігом:
– стадія компенсації;
– стадія субкомпенсації;
– стадія декомпенсації;
– термінальна стадія.
Тяжкість клінічного перебігу цирозу печінки визначається з урахуванням вираженості клініко-лабораторних даних і оцінюється за методикою, запропонованою Чайлдом і доповненої П’ю:
| Клинична класифікація (за Чайлдом-П’ю) | Пункти | ||
| 1 | 2 | 3 | |
| Асцит | Немає | Помірний | Виражений |
| ПСЕ, ст. | 0 | I–II | III–IV |
| Білірубін, мкмоль/л | <34 | 34–51 | >51 |
| Альбумін, г/л | >35 | 28–35 | <28 |
| ПТІ, % | >70 | 70–40 | <40 |
Клінічна картина
Клінічно цироз печінки проявляється наступними синдромами:
– астеновегетативним;
– диспепсичним;
– больовим;
– холестатичним;
– геморагічним;
– дисгормональним;
– суглобним;
– пропасним.
Вираженість клінічних проявів залежить від стадії захворювання, а також активності патологічного процесу. Специфічними для цирозів печінки є синдром портальної гіпертензії та печінково-клітинної недостатності.
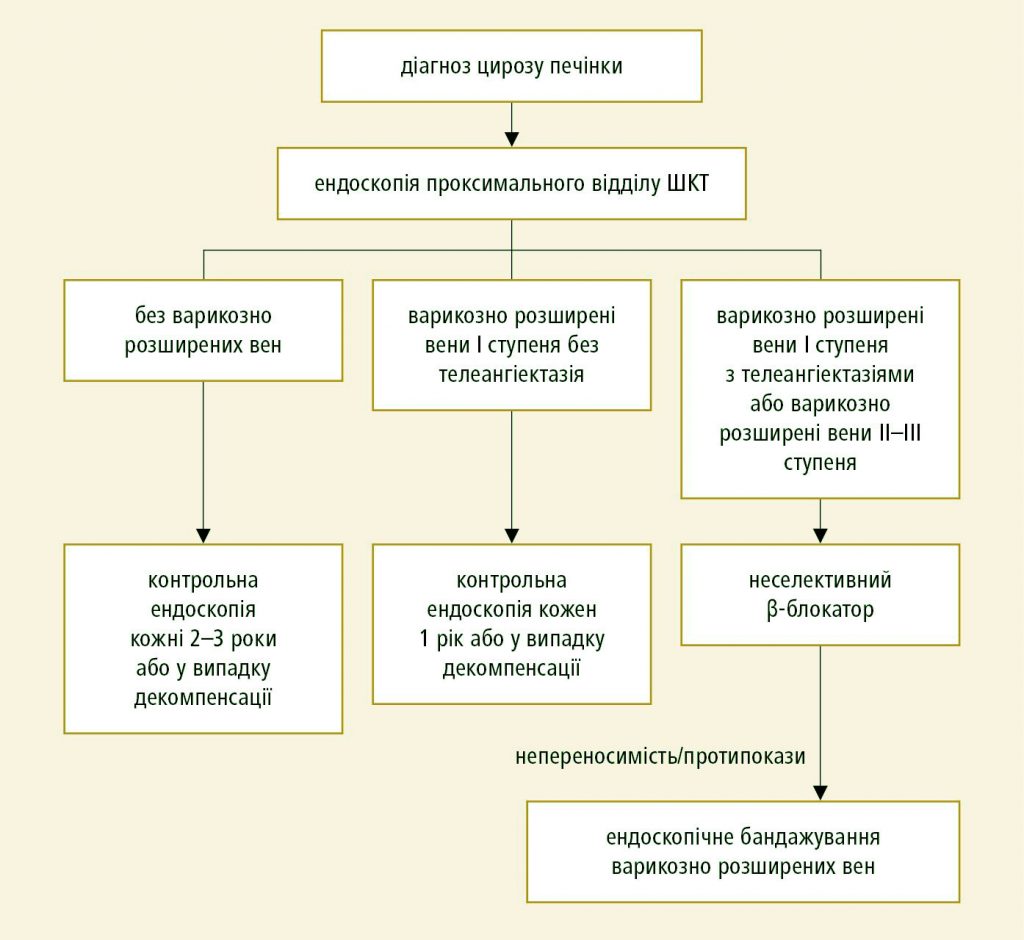
Синдром портальної гіпертензії обумовлений підвищенням тиску в системі воротної вени й проявляється гепатоспленомегалією, асцитом, розширенням подщкірних вен. Описано чотири стадії портальної гіпертензії.
Розширені підшкірні вени на передній черевній стінці живота – це анастомози між системою воротної вени та нижньої й верхньої порожніх вен при синдромі портальної гіпертензії. Анастомози навколо пупка звуться «голова медузи». По колатералях черевної стінки, розташованим вище пупка, кров з воротної вени надходить у верхню порожню вену, по коллатералях нижче пупка – у нижню порожню вену. При утрудненні току крові по нижній порожній вені розвиваються колатералі між системами нижньої й верхньої порожніх вен, що розташовуються в бічних відділах черевної стінки.
Асцит (скупчення рідини в черевній порожнині) – прояв портальної гіпертензії й ураження паренхіми печінки у вигляді рівномірно збільшеного живота, зі згладженим або випнутим пупком, стоншеною шкірою, мінливого за формою (при зміні положення тіла хворого) на тлі порівняно тонких, без набряків кінцівок. У випадку стиснення нижньої порожньої вени, поряд з асцитом, виявляють набряк нижніх кінцівок. Асцит обумовлений гіпоальбумінемією, зниженням осмотичного тиску плазми, портальною гіпертензією, підвищенням рівня альдостерону із затримкою натрію й води в організмі, підвищенням проникності мембран судин.
Асцит різного ступеня вираженості може спостерігатися при всіх формах цирозів. Можливий раптовий або поступовий, протягом декількох місяців, розвиток асциту. У 25% хворих цирозом асцит є першою ознакою захворювання.
Ранніми ознаками формування асциту є збільшення маси тіла, негативний баланс діурезу. Перкуторно виявляють притуплення перкуторного звуку над фланками й у нижній половині живота (залежно від положення тіла). Черевна стінка різко розтягнута й стоншена, на ній з’являються білі стрії, пупок випинається назовні. Підвищення внутрішньочеревного тиску сприяє утворенню гриж – пупкової і стегнової. Виражений асцит викликає підйом діафрагми з поворотом серця й зсувом верхівкового поштовху вліво, збільшенням тиску в малому колі кровообігу з набряканням шийних вен. Пропотівання асцитичної рідини в порожнину плеври через щілини в сухожильній частині діафрагми може викликати гідроторакс, частіше правобічний.
Спленомегалія – збільшення селезінки, у результаті компенсаторної імунної реакції й застійної венозної гіпертрофії, що обумовлена портальною гіпертензією. Спленомегалія є частою ознакою цирозу печінки. Розміри печінки й селезінки можуть варіювати від невеликих до вираженого збільшення.
Синдром гіперспленизму – підвищення й спотворення функції збільшеної селезінки, проявляється:анемією, лейкопенією з нейтропенією, лімфоцитопенією і тромбоцитопенією, компенсаторною активацією кісткового мозку з підвищенням кількості кліток, незрілих попередників еритроцитів і тромбоцитів.
Синдром печінково-клітинної, або гепатоцелюлярної недоста- тності, що проявляється зниженням апетиту, нудотою, непере- носимістю алкоголю, тютюну, схудненням, сухою шкірою, гіповітамінозом, лихоманкою, паренхіматозною жовтяницею, печінковим запахом з рота. Вираженість цього синдрому залежить від стадії (компенсована, субкомпенсована, декомпенсована).
Печінковий запах – солодкуватий, що відчувається при подиху хворих, обумовлений порушенням обміну амінокислот і ароматичних сполук, зокрема,продуктів перетворення метіоніну. При ендогенній комі запах схожий із запахом сирої печінки, при екзогенній – із запахом сірки або переспілих фруктів.
Гепатопанкреатичнийсиндром – зниження функції підшлункової залози.
Діагностика
У діагностиці цирозів печінки використовуються ті ж додаткові дослідження, що й при хронічних гепатитах (загальний аналіз крові, загальний аналіз сечі, біохімічне дослідження сироватки крові).
Дослідження асцитичної рідини: стерильний транссудат, відносна щільність менш 1015, вміст білка – 20-30 г/л, лейкоцити – близько 280 у мкл, у т.ч., до 27% паличкоядерних нейтрофілів, невелика кількість лімфоцитів і мезотеліальних клітин.
При оглядовій рентгенографії органів черевної порожнини визначається високе стояння купола діафрагми (при асциті).
Ультразвукове дослідження дозволяє визначити розміри печінки й селезінки, характер поверхні й нижнього краю печінки, ущільнення її капсули, поява грубих порушень ехоструктури й судинної структури органа.
Ультразвукове сканування дозволяє здійснити ранню діагностику портальної гіпертензії (найбільш ранньою морфологічною ознакою є збільшення діаметра портальної вени більш 15 мм і діаметра селезінкової вени більш 10 мм, реканалізація пупкових вен, спонтанні судинні шунти), а також виявити накопичення асцитичної рідини навіть у мінімальній кількості – спочатку навколо печінки, потім у бічних відділах живота й у маломутазі.
Комп’ютерна томограма дозволяє визначити стан і ступінь збільшення печінки й селезінки, а також наявність портальної гіпертензії, асциту.
Радіонуклідне дослідження при цирозі печінки дозволяє визначити грубі порушення основних показників кліренсу радіофармпрепарату: час напівперіоду кліренсу крові подовжується до 10 хвилин, час досягнення максимуму концентрації в паренхімі печінки – до 44 хвилин, напівперіод у екскреції фармпрепарату з печінки – до 200 хвилин. Спостерігається виражена деформація сцинтиграфічного зображення – розподіл колоїду в печінці нерівномірно, крупновогнищева нерівномірність розподілу по всьому контуру печінки (у місцях посиленого розростання сполучної тканини накопичення фармпрепарату знижене). Нерідко визначається збільшення в розмірах і більш інтенсивне зображення лівої частки, тоді як права частка зменшується в розмірах і менше накопичуєфармпрепарат.
Часто спостерігається зменшення розмірів печінки, внаслідок різкого зниження накопичення фармпрепарату в крайових зонах, при цьому розміри печінки, що визначаються даним методом і ехосонографічно, не збігаються. Характерна зміна співвідношення між накопиченням радіофармпрепарату в печінці й селезінці – нерідко інтенсивність зображення селезінки є більшою, ніж печінки. Структура селезінки стає неоднорідною, внаслідок тромбозів й вогнищ проліферації. Можливе накопичення препарату в костях хребта й таза.
Ускладнення
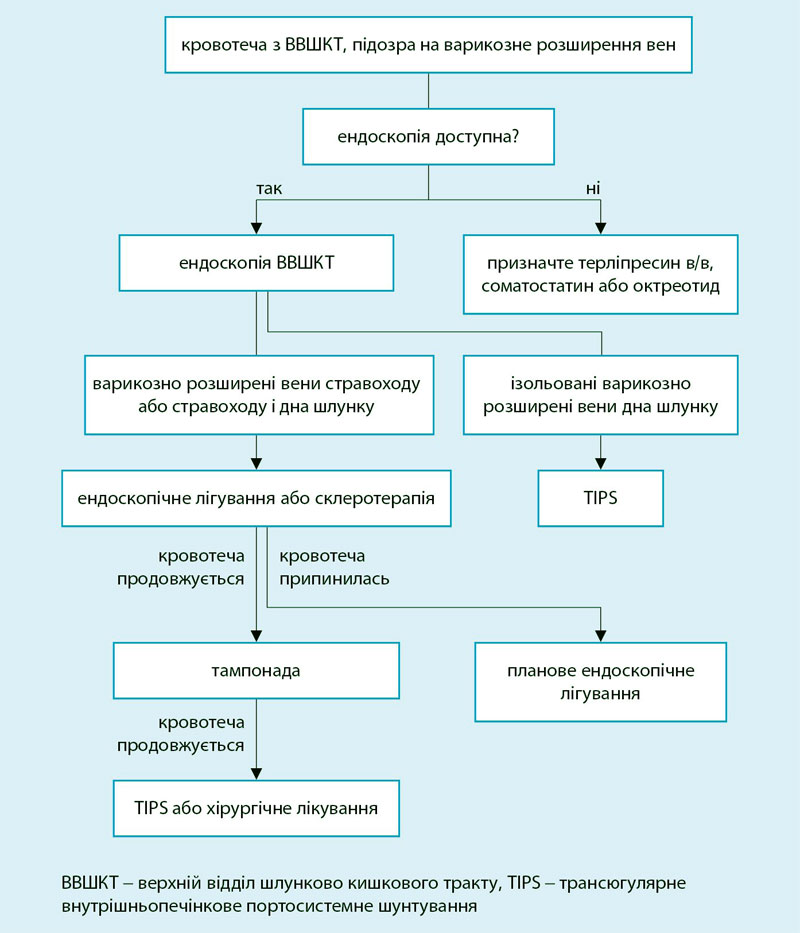
- Кровотечі із варикозно розширених вен стравоходу.
- Гепаторенальний синдром.
- Печінкова кома (гепатоцеребральна недостатність).
- Симптоматичні виразки шлунка й 12-палої кишки.
- Остеопороз і остеомаляція.
Гостра печінкова недостатність — це раптове та швидко прогресуюче погіршення функції печінки у хворих, в яких раніше не діагностовано хронічного захворювання печінки, що характеризується виникненням жовтяниці, порушень плазмового гемостазу (МНВ >1,5) та печінкової енцефалопатії.
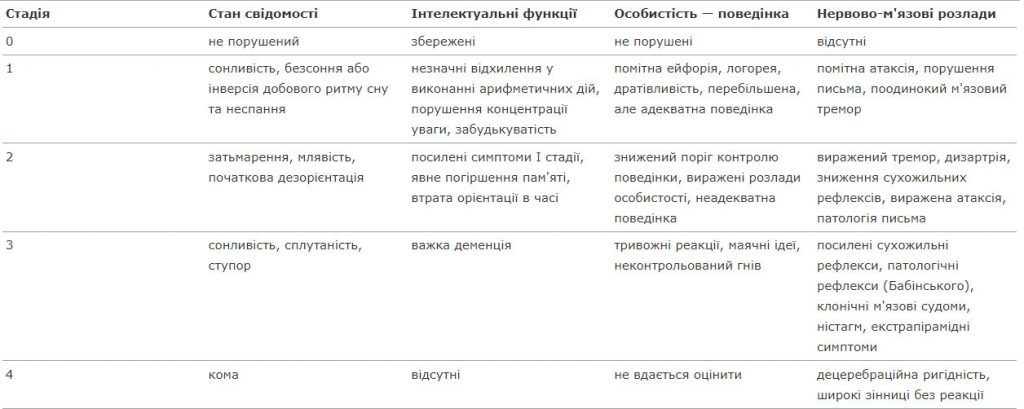
Печінкова енцефалопатія є найбільш показовим і чутливим клінічним проявом печінкової недостатності, що чітко відображає позитивну або негативну її динаміку.
Печінкова недостатність клінічно проявляється печінковою енцефалопатією (ПЕ), жовтяницею, асцитом, набряками тканин, геморагічним синдромом, гіпердинамічним типом кровообігу, пальмарною еритемою, телеангіектазіями, печінковим запахом (fetor hepaticus), ендокринними змінами, лихоманкою, септицемією.
Під симптомокомплексом «печінкова енцефалопатія» розуміють комплекс потенційно оборотних нервовопсихічних порушень, що виникають у випадках печінкової недостатності крайнього ступеня тяжкості в результаті гепатоцелюлярної недостатності або портосистемного шунтування крові.
Однією з причин гепатоцелюлярної недостатності може бути масивний некроз гепатоцитів у пацієнтів без захворювань печінки в анамнезі. У таких випадках говорять про гостру печінкову недостатність (ГПН), основною ознакою якої є ПЕ, що, у свою чергу, визначає тяжкість перебігу ГПН і прогноз захворювання. Якщо ПЕ розвивається протягом 8 тижнів від появи перших симптомів гепатоцелюлярної недостатності, то в таких випадках говорять про ГПН, а якщо в межах 7 днів — про найгостріший перебіг печінкової недостатності.
Причинами розвитку ГПН можуть бути:
- у 30–80 % випадків — інфекційні агенти, а саме: вірусні гепатити, жовта лихоманка, інші вірусні інфекції, Coxiella burnetii;
- у 5 % — токсини блідої поганки;
- в 30–50 % — хімічні реагенти і лікувальні препарати (фосфор, галогенати, гідрокарбони, ацетамінофен, тетрациклін, галотан, етанол, ізоніазид, метилдопа, інгібітори моноаміноксидази, вальпроат натрію);
- у 5 % — ішемія/гіпоперфузія та гіпоксія печінки в результаті оклюзії печінкових судин (печінкової артерії, портальної вени), шокових станів, застійної серцевої недостатності, ексудативного перикардиту;
- у 5–10 % — різноманітні метаболічні аномалії (гостра жирова дистрофія печінки вагітних, синдром Рея, єюноілеокавальне шунтування, хвороба Вільсона, галактоземія, спадкова відсутність толерантності до фруктози, спадкова тирозинемія).
Причиною портокавального шунтування крові є тривала портальна гіпертензія, в результаті якої формуються функціональні шунти між системами портального і загального кровообігу, що призводить до попадання токсичних продуктів вмісту кишечника в системний кровотік і головний мозок.
Патогенетичними факторами, що беруть участь у формуванні ПЕ, є:
— підвищення ендогенних нейротоксинів — аміаку, меркаптанів (продуктів бактеріального гідролізу сірковмісних амінокислот — метіоніну, цистеїну, цистину в товстому кишечнику, що зумовлюють появу печінкового запаху), коротко та середньоланцюжкових жирних кислот, фенолів, які гальмують синтез сечовини в печінці, витісняють триптофан із зв’язку з альбуміном, що спричинює збільшення надходження триптофану в головний мозок, де з триптофану синтезується надлишок серотоніну, що призводить до домінування серотонінергічних структур над адренергічними і клінічно може проявлятися сонливістю, поведінковими ефектами уникнення боротьби, серотонінергічною стимуляцією блювального центру;
— амінокислотний дисбаланс з підвищенням концентрації в плазмі ароматичних амінокислот (фенілаланіну, тирозину, метіоніну, триптофану) і зниженням умісту амінокислот із розгалуженим бічним ланцюжком (лейцину, ізолейцину, валіну);
— порушення балансу нейротрансмітерів у вигляді синтезу псевдонейротрансмітерів (октопамін, фенілетаноламін та ін.); пригнічення синтезу збуджуючих — дофаміну, норадреналіну; підвищення синтезу гальмівних — серотоніну, гаммааміномасляної кислоти (ГАМК);
— зміни активності рецепторів постсинаптичної мембрани під впливом пікротоксину, підвищення активності бензодіазепінових рецепторів;
— порушення функціонування гематоенцефалічного бар’єра у вигляді порушення транспорту енергетичних субстратів і підвищення його проникності.
Тривале вивчення патогенезу ПЕ дозволяє стверджувати, що вищенаведені фактори патогенезу діють спільно, викликаючи формування ПЕ. Провокуючими факторами розвитку або поглиблення прояву ПЕ можуть бути:
— підвищене надходження білка в організм за рахунок дієти, збагаченої білком (7–10 % випадків) або через шлунковокишкову кровотечу (25–30 %);
— підвищений катаболізм білка у випадках дефіциту альбуміну, лихоманки, хірургічних втручань, інфекцій, гіперглюкагонемії, розсмоктування об’ємних гематом;
— фактори, що знижують детоксикаційну функцію печінки, а саме: запор, алкоголь, медикаменти, екзо та ендотоксини, інфекції (10–18 %);
— підвищення концентрації фактора некрозу пухлини альфа;
— зв’язування рецепторів ГАМК похідними бензодіазепінів, барбітурової кислоти, фенотіазинів (10–15 %);
— метаболічні порушення, такі як ацидоз, азотемія (25–30 %), гіпоглікемія;
— електролітні порушення (гіпокаліємія, гіпонатріємія, гіпомагніємія, гіпермарганцемія);
— циркуляторні порушення: артеріальна гіпотензія, гіпоксія, гіповолемія;
— пригнічення синтезу сечовини під впливом петльових діуретиків (25–30 %), на фоні ацидозу і зниження плазматичної концентрації цинку.
За клінічним перебігом вирізняють такі форми ПЕ:
1. Синдром Рея.
2. Дефіцит ферментів орнітинового циклу: гіперамоніємія І типу, гіперамоніємія ІІ типу.
3. Псевдопортосистемна енцефалопатія.
4. Фульмінантна печінкова недостатність.
5. Портосистемна енцефалопатія: субклінічна (латентна), гостра, гостра рецидивуюча, хронічна персистуюча, хронічна рецидивуюча.
Провідну роль у патогенезі псевдопортосистемної енцефалопатії (інші назви — хибна печінкова кома, електролітна кома) відіграє електролітний дисбаланс у вигляді гіпокаліємії, гіпонатріємії або гіпомагніємії, що зумовлює розвиток гіпотонічної дегідратації клітин головного мозку. Найбільш часта причина цього — передозування петльових діуретиків.
Стадії печінкової енцефалопатії
- Встановлення супутніх захворювань
Консультації фахівців
- Консультація сімейного лікаря (обов’язково) – амбулаторне ведення пацієнта
- Консультація гастроентеролога (обов’язково) – консультація, призначення діагностики та медикаментозного лікування
- Консультація хірурга (за потреби) – консультація, призначення діагностики та обрання тактики хірургічного лікування за необхідності
- Консультація токсиколога (за потреби) – консультація, призначення діагностики та визначення токсичного агенту, призначення лікування
- Консультація невропатолога (за потреби) – діагностика та лікування неврологічних ускладнень (печінкової енцефалопатії)
- Консультація офтальмолога (за потреби) – проведення диференційної діагностики ТГ та хворобиВільсона – Коновалова
- Консультація реаніматолога (за потреби) – обрання тактики лікування при невідкладних станах
Призначення лікування
- Медикаментозне лікування
Принципи лікування ТГ такі:
- Негайно припинити використання підозрюваних токсичних препаратів, якщо вони не є критичними для контролю основного захворювання, і уникати повторного використання підозрілих препаратів або подібних токсичних агентів;
- Зважити баланс між ризиком прогресування основного захворювання після відміни препарату та ризиком загострення ураження печінки, викликаного безперервним прийомом потенційно пов’язаних препаратів;
- Лікувати ТГ відповідно до клінічних картини захворювання;
- Слід розглянути екстрену трансплантацію печінки для пацієнтів із гострою печінковою недостатністю та підгострою печінковою недостатністю.
На даний момент немає жодних доказів, які б підтверджували, що спільне застосування двох або більше типів протизапальних та гепатопротекторних препаратів підвищить терапевтичну ефективність при ТГ. Крім того, на сьогоднішній день немає жодних доказів, які б підтверджували цінність і необхідність профілактичного використання цих препаратів для зниження ризику ТГ, наприклад під час протитуберкульозної або протипухлинної терапії. Однак у цих клінічних умовах, особливо протягом перших трьох місяців протитуберкульозної терапії, дуже важливо проводити посилений моніторинг біохімічних тестів, пов’язаних з функцією печінки, щоб раніше виявити ураження та призначити раціональне лікування.
Відміна препарату
Своєчасна відміна препаратів, які передбачають ушкодження печінки, є найважливішою стратегією лікування ТГ. У більшості випадків препарати-винуватці слід відмінити негайно після їх виявлення, і приблизно у 95% пацієнтів можна досягти спонтанного покращення; більшість повністю одужує після припинення прийому препарату, але у деяких пацієнтів може розвинутися хронічний ТГ, а в деяких випадках може прогресувати печінкова недостатність. Відомо, що середній курс відновлення становив приблизно 3,3 ± 3,1 тижні для пацієнтів із гепатоцелюлярним ураженням і 6,6 ± 4,2 тижнів для пацієнтів із холестатичним ураженням.
Оскільки індивідуальна адаптація до гепатотоксичності лікарського засобу є загальною для населення, вважається, що підвищення сироваткових рівнів АЛТ або АСТ, яке становить <3 ВМН без симптомів, не обов’язково є показанням для негайної відміни препарату. Але, зокрема, ризик розвитку печінкової недостатності зростатиме при постійному застосуванні гепатотоксичних препаратів, коли загальний білірубін та/або МНВ помітно підвищуються.
Фармакотерапія
N -Ацетилцистеїн (NAC) може знижувати вільні радикали, і чим раніше він буде використаний, тим кращою буде його клінічна ефективність . Дорослим пацієнтам слід призначати NAC у дозі 50–150 мг/(кг на добу) протягом принаймні 3 днів; швидкість внутрішньовенної інфузії слід суворо контролювати, щоб уникнути побічних реакцій.
Наразі в Китаї NAC рекомендовано для лікування пацієнтів із ранньою стадією ГПН, але необхідні подальші дослідження щодо терапевтичних ефектів NAC у пацієнтів із помірним або важким ТГ. У США NAC є єдиним антидотом, схваленим у 2004 році FDA для лікування ТГ спричиненого ацетамінофеном, і, окрім ацетамінофено-індукованого ТГ, NAC рекомендований для використання пацієнтам із ГПН при інших захворюваннях.
У 2011 році Американська асоціація з вивчення захворювань печінки (AASLD) опублікувала рекомендації щодо ГПН, у яких рекомендовано використовувати NAC для лікування ГПН, спричиненої наркотиками та отруєнням блідою поганкою.
На даний момент не було рандомізованих контрольованих досліджень щодо терапевтичного ефекту глюкокортикоїдів для лікування автоімунних гепатитів, хоча вони іноді використовуються для лікування дуже важких їх форм. Враховуючи численні побічні реакції глюкокортикоїдів, їх слід застосовувати з обережністю. Теоретично та емпірично глюкокортикоїди можна призначати пацієнтам з вираженими ознаками гіперчутливості або автоімунітету, але без помітного поліпшення або навіть погіршення біохімічних показників після відміни гепатотоксичних препаратів.
На підставі висновків про те, що ізогліциризинат магнію може знижувати рівень АЛТ у сироватці крові у пацієнтів із ТГ, він був схвалений FDA для лікування гострого ТГ, включаючи форми гострого гепатоцелюлярного ураження та змішане ураження печінки зі значним підвищенням рівня AЛT у сироватці.
Емпірично, для лікування гепатоцелюлярного ураження або змішаного ураження печінки легкого та помірного ступеня тяжкості можна розглянути біциклол і гліциризинову кислоту для лікування пацієнтів із важким запаленням печінки, а також силімарин, обраний для лікування тих, хто має легке запалення печінки.
При токсичних ураженнях печінки, що супроводжуються холестазом, доцільно призначення препарату урсодезоксихолієвої кислоти, що сприяє зменшенню в ентерогепатичній циркуляції гідрофобних ЖК (тим самим запобігає їх токсичному впливу на мембрани гепатоцитів і на епітелій жовчних протоків), а також знижує аутоімунність процесу. Препарати застосовуються в дозі 10–15 мг/кг до купірування холестазу, в подальшому показано тривале лікування в підтримуючих дозах.
Адеметіонін (S-аденозил-L-метіонін, SAMe) відіграє важливу роль у ключових біохімічних процесах, зокрема, біосинтезі фосфоліпідів, синтезі глутатіону і таурину, кон’югації жовчних кислот, детоксикації жовчних кислот і ксенобіотиків, синтезі поліамінів, що мають важливе значення у формуванні структури рибосом і процесах регенерації. Такі властивості адеметіоніну, як здатність підвищувати рівень глутатіону в мітохондріях і підтримувати їх функціональну активність, інактивувати систему цитохрому Р450, пригнічувати експресію ФНП, стали підставою його широкого застосування у клінічній практиці, в тому числі при ТГ. Важливу роль у цьому аспекті відіграють антифібротичні, антинейротоксичні й антидепресивні властивості адеметіоніну. Ефективність адеметіоніну при ТГ, викликаних призначенням протипухлинних препаратів, доведена в низці досліджень. Є дані про ефективність адеметіоніну в лікуванні холестатичних форм ТГ, зумовлених застосуванням метотрексату, циклоспорину і кортикостероїдів у хворих із тяжкими формами псоріазу. Рекомендована схема призначення адеметіоніну: 1000 мг на добу внутрішньовенно протягом 2 тижнів, далі – 1000-1500 мг на добу перорально протягом 1 місяця.
Оптимально збалансованим препаратом за амінокислотним складом і кількісним співвідношенням компонентів є комбінація натуральних компонентів аргініну і бетаїну у вигляді розчину для внутрішнього застосування в ампулах по 10 мл. Аргінін — умовно незамінна амінокислота, яка бере участь у процесі ядерного і цитоплазматичного біосинтезу; відіграє важливу роль у підтримці азотистого балансу, виведенні надлишкового азоту, регуляції імунологічних реакцій; є структурним компонентом низки ферментів і гормонів.
Завдяки участі аргініну в нейтралізації аміаку підвищується детоксикаційна функція печінки, зменшується накопичення лікарських метаболітів у печінці; завдяки участі аргініну в синтезі аденозинтрифосфату — накопичується енергія в тканинах, посилюється регенерація в печінці. Крім того, амінокислота аргінін є основним субстратом або попередником оксиду азоту — потужного ендогенного вазодилататора, тому аргінін має антиоксидантну дію, поліпшує мікроциркуляцію, завдяки чому збільшується портальний кровотік, прискорюється виведення кінцевих токсинів. Такі ефекти аргініну дозволяють застосовувати його при захворюваннях печінки і пояснюють швидкість настання клінічних ефектів на тлі його прийому.
У разі розвитку гострого медикаментозного гепатиту, зумовленого прийомом лефлуноміду та тербінафіну, можна використовувати холестирамін у дозі 4 г через кожні 6 год протягом 2 тижнів, щоб прискорити виведення цих лікарських засобів.
Специфічним антидотом проти гепатотоксичності вальпроату є L-карнітин. Сприятливий вплив L-карнітину полягає у регулюванні ним мітохондріального рівня ацетил-КоА, що зумовлює посилення поглинання жирних кислот і бета-окиснення в мітохондріях. Рекомендована доза L-карнітину становить 100 мг/кг маси тіла (але менше 6 г) внутрішньовенно протягом 30 хв з подальшим прийомом по 15 мг/кг через кожні 4 год до клінічного поліпшення.
Для синдрома синусоїдальної обструкції / веноокклюзійного захворювання печінки раннє використання антикоагулянтів, таких як низькомолекулярні гепарини, може мати певний терапевтичний ефект. Для ТГ під час вагітності, окрім відміни гепатотоксичних препаратів, також слід приділяти увагу покращенню результату вагітності, запобіганню передчасним пологам та ретельному моніторингу стану плода з метою переривання вагітності в належний час.
Есенціальні фосфоліпіди (ЕФЛ) продемонстрували свою ефективність при експериментальних моделях токсичного гепатиту, індукованого прийомом парацетамолу, тетрацикліну та індометацину, що зумовило доцільність їх призначення при МУП у людей. Лікувальний ефект ЕФЛ полягає в нормалізації структури мембран та органел клітини, зменшенні та зникненні некрозу гепатоцитів, посиленні їх регенерації та зниженні інтенсивності утворення сполучної тканини. Хороший гепатопротекторний ефект отримано при використанні ЕФЛ у складі лікувальних комплексів на тлі дезінтоксикаційної терапії у пацієнтів із токсичним ураженням печінки, викликаним галогеновими вуглеводнями, фосфорорганічними пестицидами, протиепілептичними препаратами, а також у хворих онкогематологічного профілю, які отримували курси поліхіміотерапії з приводу неходжкінської лімфоми, гострого лейкозу та хронічного мієлолейкозу. Рекомендований режим застосування ЕФЛ: внутрішньовенне введення від 500 до 1000 мг протягом 7-10 днів з подальшим переходом на пероральний прийом у дозі 1800 мг/добу. Тривалість терапії визначається вираженістю цитолітичного синдрому і становить від 4 до 12 тижнів.
Глутатіон є природним компонентом клітин усіх тканин організму. Він забезпечує широкий спектр біологічних функцій і має фундаментальне значення для численних біохімічних і метаболічних процесів. Сульфгідрильні групи цистеїну, що входять до складу глутатіону, є потужними антиоксидантими агентами. У зв’язку з цим вони стають основною метою електрофільної атаки хімічних речовин або їх активних метаболітів, що призводить до інактивації потенційно токсичних екзогенних речовин. Таким чином, препарат справляє захисну дію на життєво важливі нуклеофільні ділянки, при атаці на які починається процес пошкодження клітин. Крім того, глутатіон, відновлений у результаті взаємодії з великою кількістю окиснених органічних метаболітів, утворює менш токсичні кон’юговані сполуки, які згодом легше метаболізуються і виводяться в складі меркаптурової кислоти. Глутатіон зв’язує велику кількість ліпофільних сполук, запобігаючи їх вбудовуванню в ліпідний шар мембран і порушенню функцій клітини, покращує стабільність клітинної мембрани, захищає мембрану клітин печінки, підвищує активність ферментів печінки і сприяє детоксикації та відновній активності органа шляхом знищення вільних радикалів. З урахуванням цих властивостей глутатіон призначають у разі реакцій гепатотоксичності, механізмами розвитку яких можуть бути етиловий або медикаментозний гепатотоксикоз. Препарати глутатіону вводять внутрішньовенно або внутрішньом’язово по 1-2 флакони (600-1200 мг) протягом 10-30 днів, далі – приймають перорально по 2-4 капсули (250-1000 мг) на добу впродовж 1-6 місяців. При тяжких токсичних ураженнях печінки дозу глутатіону для внутрішньовенного введення, згідно з даними рандомізованих клінічних досліджень, можна підвищувати до 2400 мг/добу.
Профілактика ТГ має включати ретельний збір анамнезу до призначення медикаментозної терапії, персоналізовану ідентифікацію пов’язаних із нею факторів ризику у конкретних пацієнтів. Важливе значення має уникнення поліпрагмазії з метою виключення міжлікарських взаємодій. У разі призначення потенційно гепатотоксичних препаратів слід проводити моніторинг лабораторних показників цитолізу та холестазу. Для запобігання ТГ за можливості слід застосовувати препарати з високим профілем безпеки. У разі призначення препаратів з потенційно високою гепатотоксичністю в окремих випадках доцільно проводити генетичні тести на індивідуальну чутливість, зокрема визначення поліморфізму генів систем біотрансформації.
- Хірургічне лікування
Трансплантація печінки повинна бути розглянута для пацієнтів із гострою та підгострою печінковою недостатністю, які мають печінкову енцефалопатію та тяжкі порушення згортання крові, а також декомпенсований цироз.
Трансплантація печінки показана пацієнтам, які відповідають, критеріям King’s College:
1) хворі з пошкодженням печінки, що спричинений парацетамолом — рН артеріальної крові <7,3 або всі з наступних критеріїв: 3 або 4 стадія енцефалопатії, протромбіновий час >100 с (МНІ >6,5), рівень креатиніну >3,4 мг/дл (301 мкмоль/л);
2) хворі з пошкодженням печінки іншої етіології — ПЧ >100 с (МНВ >6,5) або ≥3 з наступних критеріїв: вік <10 років чи >40 років, період тривання жовтяниці перед розвитком енцефалопатії >7 днів, ПЧ >50 c (МНВ >3,5), рівень білірубіну >18 мг/дл (308 мкмоль/л), етіологія (вірусний гепатит ні А ні В, галотан індукований гепатит, або ідіосинкразія на ліки).
У випадку показів до трансплантації печінки шанс на порятунок хворого існує, якщо пересадка відбудеться впродовж 48 год від звернення до координаційного центру.
Екстракорпоральна підтримка функції печінки
Найчастіше використовується при печінковій енцефалопатії з надією підтримати деякі метаболічно-детоксикаційні функції печінки до моменту трансплантації органу або одужання. Техніки:
- MARS [Molecular Adsorbent Recycling System] — метод, що поєднує альбуміновий діаліз з адсорбцією,
- печінковий діаліз (FSPA),
- альбуміновий діаліз в системі одного переходу альбумінового діалізату (SPAD),
- комбінований з постійною вено-венозною гемодіафільтрацією (CVVHDF). Однак немає переконливих даних про їх ефективність.
- Лікування ускладнень
Цироз печінки
При компенсованому цирозі печінки слід порекомендувати абсолютну відмову від алкоголю і куріння та збалансовану дієту, що забезпечує покриття добової потреби в енергії (35 ккал/кг м.т./добу) та білку (1,2–1,5 г/кг м.т./добу). Прийом 3-х основних прийомів їжі (сніданок, обід, вечеря) і 3-х перекусів у вигляді другого сніданку, післяобіднього перекусу, а особливо пізно ввечері — легкої їжі, яка складається з вуглеводів, протидіє нічному глюконеогенезу з розпаду білків, і таким чином гіпотрофії. У пацієнтів із гіпотрофією або саркопенією може бути корисним прийом із їжею рідких харчових добавок (готові харчові суміші) aбо застосування ентерального харчування, а іноді і парентерального. Немає потреби у суплементації метіоніну, ані застосування гепатопротекторів, чи препаратів розгалужених амінокислот (за винятком випадків, у яких необхідно обмежити добовий прийом білка).
Визначте концентрацію вітаміну D у сироватці крові; якщо <20 нг/мл → рекомендуйте оральні добавки (цільова концентрація >30 нг/мл). Слід заохочувати пацієнтів до фізичної активності (це запобігає втраті м’язової маси).
Симптоматичне лікування:
- гіпонатріємія з гіперволемією — є ознакою гіпергідратації; безсимптомна не вимагає лікування; при натріємії <125 ммоль/л – обмеження прийому рідини до нижчого, ніж добовий діурез, при тяжкій (<110 ммоль/л) або симптомній гіпонатріємії — поповнення натрію;
- гіпонатріємія з гіповолемією — вимагає результат недостатнього постачання або надмірної втрати натрію з сечею (передозування діуретиків); вимагає інфузії 0,9 % NaCl та лікування причини, найчастіше — відміни діуретиків;
- порушення згортання крові — не рекомендується коригування системи згортання шляхом введення напр., свіжозамороженої плазми (СЗП) пацієнтам без кровотечі або з кровотечею, не спричиненою порушеннями згортання (напр., кровотеча з варикозно розширених вен стравоходу) ані профілактична трансфузія тромбоцитарної маси у пацієнтів із цирозом печінки та кількістю тромбоцитів <50 000/мкл перед процедурами з низьким ризиком кровотечі, такими як видалення зуба, лігування варикозно розширених вен стравоходу або парацентез. У пацієнтів із тромбозом ворітної вени застосовуйте антикоагулянтну терапію (запобігає збільшенню тромбу, сприяє реканалізації): при гострому тромбозі спочатку гепарин (НФГ або НМГ), підтримуюча терапія НМГ або варфарином під контролем МНВ протягом ≥6 місяців (а в пацієнтів, які пройшли відбір до трансплантації печінки — до операції включно; застосування НОАК не рекомендується).
- гіперглікемія та цукровий діабет — зазвичай, тільки дієта, рідше — інсулінотерапія.
- інші методи неспецифічної терапії: неселективні β-блокатори при первинній і вторинній профілактиці кровотечі з варикозно розширени вен стравоходу; антибіотики для попередження розвитку ускладнень, пов’язаних із транслокацією бактерій із ШКТ; статини, напр., симвастатин 20–40 мг/добу (зменшує портальну гіпертензію). Рекомендується вакцинація проти вірусного гепатиту A і B, грипу і пневмококів.
Трансплантація печінки є основним методом лікування декомпенсованого цирозу печінки.
Алгоритм активного діагнозу варикозно розширених вен та запобігання першому епізоду кровотечі (на основі клінічних настанов ESGE 2020)
Асцит
1) у хворих з цирозом без асциту не слід обмежувати прийому рідини та натрію ані не застосовувати діуретиків з метою запобігання його виникнення;
2) асцит 1 і 2 ступеня → розпочинайте від обмеження натрію у дієті до 80–120 ммоль/добу (2–3 г натрію, тобто 4,6–6,9 г кухонної солі на добу). Якщо ефекту немає → слід розпочати прийом діуретиків: спіронолактону 100 мг 1 × на день вранці, збільшуйте дозу кожні 72 год на 100 мг, до макс. 400 мг/добу (якщо немає відповіді на нижчі дози). Якщо лікування неефективне (тобто зменшення маси тіла на <2 кг/тиж.) або є гіперкаліємія → додайте фуросемід 40 мг 1 × на день вранці, збільшуйте дозу на 40 мг/добу до макс. 160 мг/добу; якщо ефективність фуросеміду низька, його можна замінити торасемідом. У разі масивного асциту можна відразу застосувати комбіноване лікування спіронолактоном і петльовим діуретиком (у пропорції 100 мг спіронолактону і 40 мг фуросеміду, дози поступово збільшуйте до макс. 400 мг і 160 мг відповідно). Метою діуретичного лікування є зменшення маси тіла на 0,3–0,5 кг/добу у випадку ізольованого асциту або 0,8–1,0 кг/добу, якщо співіснують периферичні набряки). Після регресу асциту слід продовжувати дієту з обмеженням натрію, вживання рідин ≈1,5 л/добу та утримувати дозу діуретиків на рівні, що забезпечує від повторного накопичення рідини (контроль маси тіла кожні 1–2 дні). Перервіть терапію діуретиками при: тяжкій гіпонатріємії (<125 ммоль/л), гострому пошкодженні нирок (ГПН), посиленні печінкової енцефалопатії або неконтрольованих м’язових спазмах. У разі значної гіпокаліємії (<3 ммоль/л) перервіть прийом фуросеміду, а при концентрації калію в сироватці >6 ммоль/л → відмініть спіронолактон.
3) асцит 3 ступеня → лікувальний лапароцентез →Асцитичну рідину необхідно видалити повністю під час одного парацентезу. Процедуру можна повторювати при рецидиві асциту; вона є відносно безпечною, за умови належного наповнення судинного русла (у разі евакуації >5 л рідини слід ввести в/в 20 % розчин альбуміну в дозі 8 г альбуміну на кожен літр евакуйованої рідини). Можна її проводити пацієнтам з ідіопатичним бактеріальним перитонітом та пацієнтам з ГПН, що супроводжує цироз. Парацентез є методом вибору у хворих з гіпонатріємію, що не піддається корекції. З метою профілактики повторного накопичення асцитичної рідини слід застосувати діуретики та обмежувати введення натрію і рідин →вище.
4) резистентний асцит (неефективність лікування діуретиками, виникнення ускладнень, що перешкоджають застосуванню діуретиків в ефективних дозах, або швидкий, тобто протягом місяця, рецидив асциту після лікування)→TIPS (але підвищує ризик енцефалопатії), трансплантація печінки або дренування черевної порожнини. У 20–25 % хворих з резистентним асцитом спостерігається гіпонатріємія <130 ммоль/л (внаслідок посилення реабсорбції води в ниркових збірних канальцях через надлишок циркулюючого антидіуретичного гормону) → обмежте споживання рідини до <1,5 л/добу, а якщо концентрація натрію становить <125 ммоль/л → припиніть застосування діуретиків.
Еквівалентом асциту є наявність транссудату в плевральних порожнинах, особливо з правої сторони (виключте серцеву недостатність і захворювання легенів і плеври). Це прогностично несприятливий симптом; є показанням для трансплантації печінки. У пацієнтів із задишкою виконайте плевральну пункцію та дренуйте рідину під час одноразових процедур (тривале дренування протипоказано через ризик ускладнень, у тому числі інфекції). Плевродез показаний лише пацієнтам, які не пройшли відбір для трансплантації печінки або TIPS.
Спонтанний бактеріальний перитоніт (Спостерігається у 10–30 % хворих із асцитом). Лікування: необхідно негайно розпочати емпіричну антибіотикотерапію → цефотаксим в/в 2 г кожні 8–12 год; у випадку алергії на цефалоспорини ципрофлоксацин в/в або п/о 0,4–0,5 г кожні 12 год; слід продовжувати до моменту зникнення клінічних симптомів або зменшення кількості нейтрофілів в асцитичній рідині до <250/мкл (зазвичай впродовж 10–14 днів). У хворих з концентрацією білірубіну в крові >68 мкмоль/л (4 мг/дл) та креатиніну >88,4 мкмоль/л (1 мг/дл) крім антибіотикотерапії слід застосувати інфузію розчину альбуміну (1,5 г/кг м. т. в 1-ий день, а потім 1 г/кг маси тіла на 3-ій день).
Профілактика:
1) після епізоду СБП рекомендується приймати норфлоксацин п/о 400 мг/добу;
2) норфлоксацин п/о 400 мг/добу до моменту клінічного поліпшення та зникнення асциту у хворих, що мають високий ризик СБП, тобто
а) кровотеча з ШКТ в анамнезі, незалежно від причини;
б) концентрація білка в асцитичній рідині <1 г/дл; або
в) ≥9 балів за шкалою Чайлда-П’ю і концентрація сироваткового білірубіну ≥3 мг/дл (51 мкмоль/л), концентрація білка в асцитичній рідині <1,5 г/дл та порушення функції нирок або гіпонатріємія)
3) інгібітори протонної помпи призначайте лише тоді, коли існують конкретні покази, оскільки збільшують ризик розвитку СБП та ризик інфекції C. difficile.
Кровотеча ШКТ
Алгоритм дій при кровотечі з варикозно розширених вен стравоходу
1. Лікування у реанімаційно-хірургічній частині відділення невідкладної медичної допомоги, потім — у ВІТ. У хворих із значною втратою крові і розладами свідомості слід підтримувати прохідність дихальних шляхів; при необхідності проведіть інтубацію; у зв’язку з ризиком аспірації не можна зволікати з інтубацією до моменту критичного погіршення стану хворого.
2. Слід виміряти артеріальний тиск; якщо він у нормі → потрібно виміряти артеріальний тиск у вертикальному положенні. Перевірте чи є симптоми гіпоперфузії, напр., збільшене капілярне наповнення та інші симптоми шоку. Хворим із такими симптомами проводять протишокові заходи, зокрема призначають кисень у концентрації 60–100 %.
3. Відновлення об’єму втраченої крові — введіть у периферичні вени 2 канюлі великого діаметру (≥1,8 мм [≤16 G]) і переливайте розчин кристалоїдів (3 мл на кожен мл втраченої крові) або колоїду (1 мл на кожен мл втраченої крові). Якщо втрата крові оцінюється на >1/3 (>1500 мл) → також переливайте ЕМ або цільну консервовану кров. У хворих зі стабільною гемодинамікою зазвичай підтримуйте концентрацію гемоглобіну ≥7–8 г/дл.
4. Слід якнайшвидше (у разі масивної кровотечі з верхнього відділу ШКТ — після стабілізації стану хворого, в інших випадках до 24 год) зробити ендоскопію зі спробою припинення кровотечі — обколювання судиннозвужуючими або облітеруючими судини (склеротерапія) ЛЗ, електрокоагуляція, аргоноплазмова коагуляція, накладення гумових кілець на варикозно розширені вени.
5. У випадку кровотечі з варикозно розширених вен стравоходу, якщо спроба ендоскопічного припинення кровотечі виявиться невдалою, до стравоходу і шлунка можна ввести зонд Сенгстакена-Блекмора або інший зонд з балонами, що затискають розширені вени (напр. Лінтона-Нахласа); застосовуйте його впродовж не більше 24 год.
Схема правильного встановлення зонду Сенгстакена-Блекмора
Застосуйте фармакологічне лікування
1) при кровотечі з виразок шлунка чи дванадцятипалої кишки, або кровотечі внаслідок гострої геморагічної гастропатії — інгібітор протонної помпи (ІПП) в/в (езомепразол, омепразол або пантопразол) він’єкції 80 мг (2 амп.), потім — у постійній інфузії 8 мг/год впродовж 3 діб (також після ендоскопічного припинення кровотечі). Пізніше ІПП п/о (ЛЗ →розд. 4.7) 20–40 мг 1 × на день впродовж 4 тиж. (якщо результат тесту на наявність H. pylori позитивний — впродовж перших 14 днів разом з іншими ЛЗ, що необхідні для його ерадикації), після того потрібно провести ендоскопічну перевірку загоєння виразки (а також, чи ерадикація була ефективною).
2) при кровотечі із варикозно розширених вен стравоходу чи шлунка — призначте в/в один з ЛЗ, що знижують портальний тиск:
а) терліпресин, синтетичний аналог вазопресину, що має менше побічних дій — 5–20 мкг/хв у 20–40-хвилинній інфузії, а при потребі повторюйте кожні 8 год, максимально впродовж 5 днів, або ін’єкції по 1–2 мг кожні 4–6 год;
б) соматостатин — ін’єкція 250 мкг, потім постійна інфузія 250 мкг/год впродовж 5 днів;
в) октреотид — ін’єкція 50 мкг, потім постійна інфузія 50 мкг/год впродовж 5 днів;
3) у хворих, які приймають антикоагулянти, нейтралізуйте їхню дію.
У випадку неефективності ендоскопічних і фармакологічних методів зважте можливість виконання вісцеральної ангіографії і селективної емболізації кровоточивої судини або введення терліпресину у просвіт вісцеральних судин.
Зважаючи на те, що може виникнути необхідність виконання ургентної хірургічної операції, співпрацю з хірургом слід розпочати на ранньому етапі лікування. Показання до хірургічного лікування: неконтрольована масивна кровотеча (тобто така, що спричиняє нестабільність гемодинаміки); також після спроби ендоскопічного припинення; рецидивна кровотеча (після 2-х ендоскопічних втручань); тривала кровотеча, що супроводжувалась крововтратою, яку оцінено на >50 %; повторна госпіталізація з приводу кровоточивої виразки.
Хірургічне лікування:
1) кровотечi з виразки дванадцятипалої кишки → зазвичай стовбурова ваготомія з пілоропластикою, поєднаною із ушиванням кровоточивої виразки, або резекцією антральної частини з ушиванням кровоточивої виразки;
2) кровотечi з виразки або ерозій шлунка → резекційні втручання різного, залежного від ситуації і стану пацієнта характеру і об’єму;
3) кровотечi з варикозно розширених вен стравоходу → малоінвазивним методом є трансюгулярне внутрішньопечінкове портосистемне шунтування (TIPS), а у випадку його неефективності можна виконати порто-системні анастомози хірургічно або провести операцію реваскуляризації і транссекції (розтину і зшивання) стравоходу та спленектомію;
4) кровотечi з нижнього відділу ШКТ → колоноскопія, керована хірургом під час операції, інколи дозволяє локалізувати місце кровотечі; якщо це вдається — виконують сегментарну резекцію кишки з анастомозом; якщо немає можливості локалізувати кровотечу в межах товстого кишківника, виконується його субтотальна резекція з формуванням ілеоанального анастомозу.
Алгоритм дії при кровотечах з виразки
Лікування печінкової енцефалопатії
1. Дієтотерапія.
З метою зниження вмісту аміаку в крові необхідно зменшувати кількість білка в харчовому раціоні (до 40 г на день). У більшості випадків хворі з помірною хронічною печінковою енцефалопатією здатні переносити дієту, яка містить 60-80 г білка на добу. При поліпшенні стану хворого вміст білка в дієті збільшують поступово до 80-90 г/добу. Добове споживання білка можна підтримувати на рівні 1,0-1,5 г/кг, залежно від стану пацієнта та його здатності переносити такий харчовий раціон.
Збільшення вмісту білка в дієті приводить до погіршення стану у 35% пацієнтів з гострою печінковою недостатністю. Хворим рекомендується приймати їжу невеликими порціями. Це дозволяє попередити загострення печінкової енцефалопатії. У харчовий раціон рекомендується включати рослинні продукти, що містять білок; приймати харчові добавки, що містять амінокислоти з розгалуженими ланцюгами.
Після зникнення симптомів енцефалопатії можна відновити нормальний вміст білка в харчовому раціоні. Від тривалого обмеження харчового білка слід утриматися настільки, наскільки це можливо, тому що у хворих є дефіцит білка. Необхідно тривало обмежувати сіль у їжі, так як це знижує ймовірність повторного розвитку асциту. Необхідно пам’ятати, що тривале обмеження білка в їжі призводить до порушень харчування. У деяких випадках епізоди печінкової енцефалопатії повторюються після підвищення вмісту білка в харчовому раціоні. Такі хворі потребують тривалого прийому лактулози і призначення безбілкової дієти.
2. Очищення кишечника.
Для зниження вмісту аміаку рекомендуються клізми або застосування проносних засобів для очищення кишечника. Важливо забезпечувати спорожнення кишечника не менше 2 разів на день. З цією метою призначається лактулоза (Дюфалак, Нормазе) по 30-50 мл всередину кожну годину до появи діареї, потім по 15-30 мл 3-4 рази на день. Для використання в клізмі розводять 300 мл сиропу препарату в 700 мл води і заповнюють усі відділи товстого кишечника. Перед випискою пацієнта зі стаціонару дозу лактулози слід зменшити до 20-30 мл на ніч з можливою подальшою відміною на амбулаторному етапі.
3. Антибактеріальна терапія.
Неоміцин 1 г всередину 2 рази на день; метронідазол 250 мг всередину 3 рази на день; ампіцилін (Ампіциліну тригідрат) по 0,5 г 3-4 рази на день або ванкоміцин (Ванкоцін) 1 г всередину 2 рази на день . Препарати застосовуються під контролем функції нирок. Пацієнтам з печінковою недостатністю 3 і 4 стадій рекомендується катетеризація сечового міхура.
4. При гіпоглікемії і гіпокаліємії 10% розчин глюкози вводиться в / в зі швидкістю 100мл/час з хлористим калієм (40ммоль/л), але при різко вираженій гіпоглікемії використовується 25-40% розчин глюкози.
5. При гіпераммоніємії використовується орнитин (Гепа-Мерц). Препарат виявляє гепатопротекторну дію. Утилізує амонійні групи у синтезі сечовини (орнітиновий цикл), знижує концентрацію аміаку в плазмі. Сприяє нормалізації КОС організму. Застосовується всередину, в/м, в/в (струминно, краплинно). Всередину – по 3-6 г 3 рази на день після їжі. Парентерально – попередньо розчиняючи 2 г в 10 мл води для ін’єкцій: в / м – по 2-6 г на добу; в / в струминно – по 2-4 г на добу; кратність введення – 1-2 рази на добу. При необхідності – в / в крапельно: 25-50 г препарату розводять у 0,5-1,5 л 0.9% розчину NaCl, 5% розчину глюкози або дистильованої води. Максимальна швидкість інфузії – 40 крап./хв. Тривалість лікування визначається динамікою концентрації аміаку в крові та станом хворого. Курс лікування можна повторювати кожні 2-3 міс.
При гіпераммоніємії також рекомендується введення цинку сульфату (Цинктерал) внутрішньо перед їжею (дорослим 0,4-1,2 г на добу в 3 прийоми).
6. Якщо у пацієнта спостерігається виражене рухове занепокоєння і прояв печінкової енцефалопатії, то в якості седативного засобу йому можна призначити галоперидол.
При наявності ознак ураження ЦНС слід уникати призначення бензодіазепінів. Однак, якщо хворий перестав вживати алкоголь і у нього є симптоми печінкової енцефалопатії, то можна застосовувати бензодіазепіни в комбінації з лактулозою та іншими препаратами для лікування енцефалопатії.
Пацієнти, з печінковою енцефалопатією 3 і 4 ступеня важкості повинні проходити лікування в реанімації. У них високий ризик аспірації. Тому їм необхідно провести профілактичну ендотрахеальну інтубацію.
Виписати пацієнта зі стаціонару можна тільки після того, як стабілізуються вага, стан ЦНС, буде підібрана адекватна доза діуретиків.
Консультування та підтримка
- Поясніть пацієнту результати діагностичних тестів та встановлену підозру на токсичний гепатит
- Розкажіть пацієнту про природу захворювання, його можливі причини та перебіг.
- Визначте план регулярного спостереження та контролю симптомів.
- Забезпечте пацієнта інформацією про рекомендований режим дня, раціон харчування та фізичну активність.
- Підкресліть важливість звітування про будь-які зміни в симптомах та ефективності лікування.
- Відповідайте на запитання пацієнта та надавайте підтримку у вигляді посилань на релевантні джерела інформації або підтримуючих груп.
- Обговоріть різні методи лікування, включаючи медикаментозні та хірургічні методи.
- Заплануйте регулярні візити для оцінки ефективності лікування, контролю симптомів та визначення подальших кроків.
| Пояснення процедури аналізу крові на печінкові проби | Сьогодні я хочу пояснити Вам процедуру аналізу крові на печінкові проби, яка допоможе нам отримати інформацію про стан Вашої печінки. Цей аналіз, також відомий як біохімічний аналіз крові, дозволяє визначити рівні різних речовин у Вашій крові, які можуть вказувати на порушення роботи печінки. Ми будемо звертати особливу увагу на такі показники, як амінотрансферази (АЛТ та AСT), білірубін, тощо. Спосіб проведення аналізу простий та безболісний. Ми візьмемо невелику кількість крові з Вашої вени, зазвичай з плечової частини руки. Це займе всього кілька хвилин. Після цього ми відправимо отриману кров до лабораторії для аналізу. Напередодні проведення аналіза ми рекомендуємо утриматися від їжі, оскільки вона може впливати на деякі результати. Будь ласка, повідомте нас, якщо Ви приймаєте будь-які ліки. Після того, як ми отримаємо результати, ми Вас повідомимо та обговоримо їх разом. Це допоможе нам краще зрозуміти стан Вашого здоров’я та вжити необхідні заходи, якщо це буде потрібно. Цей аналіз є важливим етапом у вивченні Вашого здоров’я, і він допоможе нам вчасно реагувати на можливі аномалії у роботі печінки. Якщо у Вас є будь-які питання чи є що розповісти про своє самопочуття, будь ласка, не соромтеся розповісти нам. |
| Поясніть пацієнту результати діагностичних тестів та встановлену підозру на токсичний гепатит | AСT і AЛT – це ферменти, які знаходяться в клітинах печінки. Їхні рівні в крові можуть свідчити про стан органу. Зазвичай вони знаходяться всередині клітин, але якщо є які-небудь ускладнення або пошкодження печінки, вони можуть потрапити до крові. У Вашому випадку ми виявили підвищені рівні AСT і AЛT. Це може бути пов’язано з токсичним гепатитом, що означає, що Ваша печінка може бути пошкоджена токсичними речовинами, такими як ліки чи інші хімічні речовини. Наразі наша мета – визначити, як краще допомогти Вашій печінці відновитися. Ми можемо розглядати фактори, що спричинили цей стан та призначити лікування відповідно до конкретних обставин Вашого стану. |
| Розкажіть пацієнту про природу захворювання, його можливі причини та перебіг. | Токсичний гепатит — це запалення печінки в результаті реакції на певні речовини, яким приймалися. Токсичний гепатит може бути викликаний алкоголем, хімічними речовинами, ліками або харчовими добавками. У деяких випадках токсичний гепатит розвивається протягом кількох годин або днів після впливу токсину. В інших випадках можуть знадобитися місяці регулярного використання, перш ніж з’являться ознаки та симптоми. Симптоми токсичного гепатиту часто зникають, коли припиняється вплив токсину. Але токсичний гепатит може назавжди пошкодити печінку, що призведе до незворотного рубцювання печінкової тканини (цирозу) і в деяких випадках до печінкової недостатності, яка може бути небезпечною для життя. Легкі форми токсичного гепатиту можуть не викликати жодних симптомів і можуть бути виявлені лише за допомогою аналізу крові. Коли виникають ознаки та симптоми токсичного гепатиту, вони можуть включати: Пожовтіння шкіри та білків очей (жовтяниця) Свербіж шкіри Біль у верхній правій частині живота Втома Втрата апетиту Нудота і блювання Висип Лихоманка Втрата ваги Темна сеча або сеча кольору чаю Передозування деяких ліків, таких як ацетамінофен (тайленол, інші), може призвести до печінкової недостатності. Негайно зверніться за медичною допомогою, якщо Ви вважаєте, що дорослий або дитина прийняли передозування ацетамінофену. Ознаки та симптоми можливого передозування ацетамінофену включають: Втрата апетитуНудота і блюванняБіль у верхній частині животаКома |
| Визначте план регулярного спостереження та контролю симптомів. | План спостереження пацієнта із токсичним гепатитом зазвичай розробляється індивідуально для кожного пацієнта з урахуванням ступеня та характеру захворювання, а також реакції на лікування. |
| Забезпечте пацієнта інформацією про рекомендований режим дня, раціон харчування та фізичну активність. | Режим дня та харчування грають важливу роль у підтримці здоров’я пацієнтів з токсичним гепатитом. Однак важливо зауважити, що поради щодо харчування та режиму дня повинні бути індивідуалізованими, оскільки вони можуть залежати від конкретних обставин та рекомендацій лікаря. Ось що ми можемо Вам порекомендувати: Режим дня: Спокій та відпочинок: Забезпечте достатню кількість сну та відпочинку для підтримки відновлення організму. Фізична активність: Уникайте важких фізичних навантажень, особливо в період загострення симптомів. Уникання стресу: Спробуйте уникати стресових ситуацій, які можуть негативно впливати на організм. Харчування: Виключення токсинів: Уникайте споживання алкоголю та інших токсичних речовин. По можливості призупиніть прийом певних ліків, які можуть бути токсичними для печінки. Достатнє споживання рідини: Забезпечте достатнє споживання води для забезпечення гідратації організму. Збалансоване харчування: Включайте в раціон різноманітні продукти, багаті вітамінами та мінералами. Обмежте споживання продуктів, багатих насиченими жирами та холестерином. Легкі прийоми їжі: Обирайте легкі та легкозасвоювані страви, особливо під час загострення симптомів. Режим їжі: Розподіліть прийом їжі на декілька невеликих прийомів протягом дня замість декількох великих. Обмеження солі та цукру: Обмежте споживання солі та цукру, особливо у випадку наявності ускладнень, таких як асцит (накопичення рідини в черевній порожнині). |
| Підкресліть важливість звітування про будь-які зміни в симптомах та ефективності лікування. | Ми просимо Вас повідомляти нам про розвиток у Вас будь-яких можливих нових скарг та симптомів. Повідомляти нам про необхідність прийому будь-яких нових препаратів. |
| Відповідайте на запитання пацієнта та надавайте підтримку у вигляді посилань на релевантні джерела інформації або підтримуючих груп. | Ось ресурси, з якими ми можемо порадити ознайомитися: Mayo Clinic – Toxic Hepatitis Mayo Clinic надає легко зрозумілу та детальну інформацію щодо симптомів, причин та лікування токсичного гепатиту. American Liver Foundation – Hepatitis American Liver Foundation пропонує розділ, який охоплює різні типи гепатиту, включаючи токсичний гепатит. MedlinePlus – Drug–Induced Liver Disease MedlinePlus, створений Національною бібліотекою медицини США, має інформацію про токсичні ураження печінки та хвороби, спричинені ліками. Cleveland Clinic – Hepatitis Cleveland Clinic надає вичерпну інформацію про різні типи гепатиту, включаючи токсичний гепатит. WebMD – Hepatitis Health Center WebMD пропонує розділ про гепатит з корисною інформацією та рекомендаціями. Ми рекомендуємо завжди консультуватися з медичним фахівцем перед будь-якими кроками щодо лікування та підтримки. |
| Обговоріть різні методи лікування, включаючи медикаментозні та хірургічні методики | Ми працюватимемо, щоб визначити, що спричиняє пошкодження Вашої печінки. Іноді стає одразу зрозуміло, що спричиняє Ваші симптоми, а іноді потрібно більше дослідницької роботи, щоб визначити причину. У більшості випадків припинення впливу токсину, що викликає запалення печінки, зменшить ознаки та симптоми, які Ви відчуваєте. Лікування токсичного гепатиту може включати: Підтримуючий догляд. Пацієнти з важкими симптомами, швидше за все, отримають підтримуючу терапію в лікарні, включаючи внутрішньовенне введення рідини та ліки для полегшення нудоти та блювоти. Ваш лікар також спостерігатиме за пошкодженням печінки. Якщо ваше пошкодження печінки було спричинене передозуванням ацетамінофену, ви негайно отримаєте хімічну речовину під назвою ацетилцистеїн. Чим раніше буде введено цей препарат, тим більше шансів обмежити пошкодження печінки. Він найбільш ефективний, якщо його ввести протягом 16 годин після передозування ацетамінофену. Невідкладна допомога. Для пацієнтів, які передозували токсичні ліки, необхідна невідкладна допомога. Люди, які передозували певні ліки, крім ацетамінофену, можуть отримати користь від лікування, спрямованого на видалення шкідливого препарату з організму або зменшення його токсичної дії. Пересадка печінки. Якщо функція печінки серйозно порушена, трансплантація печінки може бути єдиним вибором для деяких пацієнтів. Трансплантація печінки — це операція з видалення Вашої хворої печінки та заміни її здоровою печінкою від донора. Більшість печінки, яка використовується для трансплантації печінки, походять від померлих донорів. У деяких випадках печінка може бути отримана від живих донорів, які жертвують частину своєї печінки. |
| Заплануйте регулярні візити для оцінки ефективності лікування, контролю симптомів та визначення подальших кроків. | Огляд сімейного лікаря 3 -4 рази на рік (залежить від тяжкості процесу)Огляд суміжних спеціалістів – за показаннямиАналіз крові на білірубін, холестерин, загальний аналіз крові, осадові проби, АСТ та АЛТ – 1 раз на рікАналіз крові з підрахуванням тромбоцитів – 4 рази на рік (при цирозі) Додаткові інструментальні методи дослідження – за показаннями. |
Завершення консультації
- Проведіть узагальнення отриманих даних та запитайте пацієнта, чи ніщо важливе не пропущене
- Поінформуйте пацієнта щодо подальшої тактики
- Подякуйте пацієнту
- Утилізуйте ЗІЗ належним чином і помийте руки
Ключові комунікативні навички
Активне слухання
Підбиття підсумків
Виділення вказівних знаків
Зареєструйтеся на нашому сайті прямо зараз, щоб мати доступ до більшої кількості навчальних матеріалів!
Підписатися на наші сторінки:
Джерела
- Kim JH. [Diagnosis of Autoimmune Hepatitis]. Korean J Gastroenterol. 2023 Feb 25;81(2):66-71. Korean. doi: 10.4166/kjg.2023.001. PMID: 36824034.
- Treem WR, Palmer M, Lonjon-Domanec I, Seekins D, Dimick-Santos L, Avigan MI, Marcinak JF, Dash A, Regev A, Maller E, Patwardhan M, Lewis JH, Rockey DC, Di Bisceglie AM, Freston JW, Andrade RJ, Chalasani N. Consensus Guidelines: Best Practices for Detection, Assessment and Management of Suspected Acute Drug-Induced Liver Injury During Clinical Trials in Adults with Chronic Viral Hepatitis and Adults with Cirrhosis Secondary to Hepatitis B, C and Nonalcoholic Steatohepatitis. Drug Saf. 2021 Feb;44(2):133-165. doi: 10.1007/s40264-020-01014-2. Epub 2020 Nov 3. PMID: 33141341; PMCID: PMC7847464.
- Sarin SK, Choudhury A, Sharma MK, Maiwall R, Al Mahtab M, Rahman S, Saigal S, Saraf N, Soin AS, Devarbhavi H, Kim DJ, Dhiman RK, Duseja A, Taneja S, Eapen CE, Goel A, Ning Q, Chen T, Ma K, Duan Z, Yu C, Treeprasertsuk S, Hamid SS, Butt AS, Jafri W, Shukla A, Saraswat V, Tan SS, Sood A, Midha V, Goyal O, Ghazinyan H, Arora A, Hu J, Sahu M, Rao PN, Lee GH, Lim SG, Lesmana LA, Lesmana CR, Shah S, Prasad VGM, Payawal DA, Abbas Z, Dokmeci AK, Sollano JD, Carpio G, Shresta A, Lau GK, Fazal Karim M, Shiha G, Gani R, Kalista KF, Yuen MF, Alam S, Khanna R, Sood V, Lal BB, Pamecha V, Jindal A, Rajan V, Arora V, Yokosuka O, Niriella MA, Li H, Qi X, Tanaka A, Mochida S, Chaudhuri DR, Gane E, Win KM, Chen WT, Rela M, Kapoor D, Rastogi A, Kale P, Rastogi A, Sharma CB, Bajpai M, Singh V, Premkumar M, Maharashi S, Olithselvan A, Philips CA, Srivastava A, Yachha SK, Wani ZA, Thapa BR, Saraya A, Shalimar, Kumar A, Wadhawan M, Gupta S, Madan K, Sakhuja P, Vij V, Sharma BC, Garg H, Garg V, Kalal C, Anand L, Vyas T, Mathur RP, Kumar G, Jain P, Pasupuleti SSR, Chawla YK, Chowdhury A, Alam S, Song DS, Yang JM, Yoon EL; APASL ACLF Research Consortium (AARC) for APASL ACLF working Party.. Acute-on-chronic liver failure: consensus recommendations of the Asian Pacific association for the study of the liver (APASL): an update. Hepatol Int. 2019 Jul;13(4):353-390. doi: 10.1007/s12072-019-09946-3. Epub 2019 Jun 6. Erratum in: Hepatol Int. 2019 Nov;13(6):826-828. PMID: 31172417; PMCID: PMC6728300.
- Newsome PN, Cramb R, Davison SM, Dillon JF, Foulerton M, Godfrey EM, Hall R, Harrower U, Hudson M, Langford A, Mackie A, Mitchell-Thain R, Sennett K, Sheron NC, Verne J, Walmsley M, Yeoman A. Guidelines on the management of abnormal liver blood tests. Gut. 2018 Jan;67(1):6-19. doi: 10.1136/gutjnl-2017-314924. Epub 2017 Nov 9. PMID: 29122851; PMCID: PMC5754852.
- Yu YC, Mao YM, Chen CW, Chen JJ, Chen J, Cong WM, Ding Y, Duan ZP, Fu QC, Guo XY, Hu P, Hu XQ, Jia JD, Lai RT, Li DL, Liu YX, Lu LG, Ma SW, Ma X, Nan YM, Ren H, Shen T, Wang H, Wang JY, Wang TL, Wang XJ, Wei L, Xie Q, Xie W, Yang CQ, Yang DL, Yu YY, Zeng MD, Zhang L, Zhao XY, Zhuang H; Drug-induced Liver Injury (DILI) Study Group; Chinese Society of Hepatology (CSH); Chinese Medical Association (CMA). CSH guidelines for the diagnosis and treatment of drug-induced liver injury. Hepatol Int. 2017 May;11(3):221-241. doi: 10.1007/s12072-017-9793-2. Epub 2017 Apr 12. PMID: 28405790; PMCID: PMC5419998.
- https://empendium.com/ua/chapter/B27.II.7.13.
- Кушнір І. Е. Медикаментозне ураження печінки: епідеміологія, клінічні прояви, діагностичні критерії та принципи лікування [Електронний ресурс] / І. Е. Кушнір // https://health-ua.com/. – 2020. – Режим доступу до ресурсу: https://health-ua.com/article/50287-medikamentozne-urazhennya-pechnki-epdemologya-klnchn-proyavi-dagnostichn-kr.
- Основні клінічні й лабораторні прояви хронічних гепатитів та цирозів печінки: метод. вказ. до практичних занять з пропедевтики внутрішньої медицини для студентів медичних факультетів вищих медичних навчальних закладів III-IV рівнів акредитації /Уклад.: Т.В. Ащеулова, Н.І. Питецька.- Харків: ХНМУ, 2018.- 16 с.
Пояснення процедури гастроскопії (ендоскопії)
Початок консультації Вимийте руки та використайте засоби індивідуального захисту, якщо це необхідно. Представтеся пацієнту, вказавши…
Модель термінальної стадії захворювання печінки за оцінкою MELD для пацієнтів віком від 12 років: Онлайн калькулятор
Оцінка MELD (Model For End-Stage Liver Disease, модель термінальної стадії захворювання печінки для пацієнтів віком…
Інтерактивний Чек-лист диференційних діагнозів при лікарсько-індукованих ураженнях печінки
Диференціальні діагнози при лікарських ураженнях печінки: Чек-лист диференціальних діагнозів лікарсько-індукованих уражень печінки (DILI) та рослинних…
Шкала RUCAM для оцінки ймовірності медикаментозного ураження печінки DILI/HILI
Шкала RUCAM (Roussel Uclaf Causality Assessment Method) допомагає провести оцінку ймовірності лікарського ураження печінки (Drug…
R-значення для оцінки типу ураження печінки онлайн калькулятор
Може використовуватися у пацієнтів з підозрою на лікарське ураження печінки (DILI) при підвищенні біохімічних показників…
Шкала Чайлд-П’ю для оцінки смертності від цирозу печінки: онлайн калькулятор
Оцінка Чайлд-П’ю може бути корисною для прогнозу пацієнтів з цирозом печінки, але новіші оцінки, такі…